本文轉載自中央研究院「研之有物」,為「中研院廣告」
- 採訪撰文/林承勳
- 責任編輯/簡克志
- 美術設計/蔡宛潔
陳律佑是中央研究院分子生物研究所的副研究員,長期致力於端粒研究,並在該領域取得了豐碩的成果。此外,他也與臨床醫療機構合作,為兒童癌症治療制定一系列計畫。然而,即使是像陳律佑這樣的研究人才,也不是在一開始就確定自己想要投入的領域,他在學生時期經歷了一段自我探索的過程。他是怎樣一步步走進端粒研究?又是什麼機緣,促成學術研究與臨床醫療合作?請跟著中研院研之有物專訪一起看看。

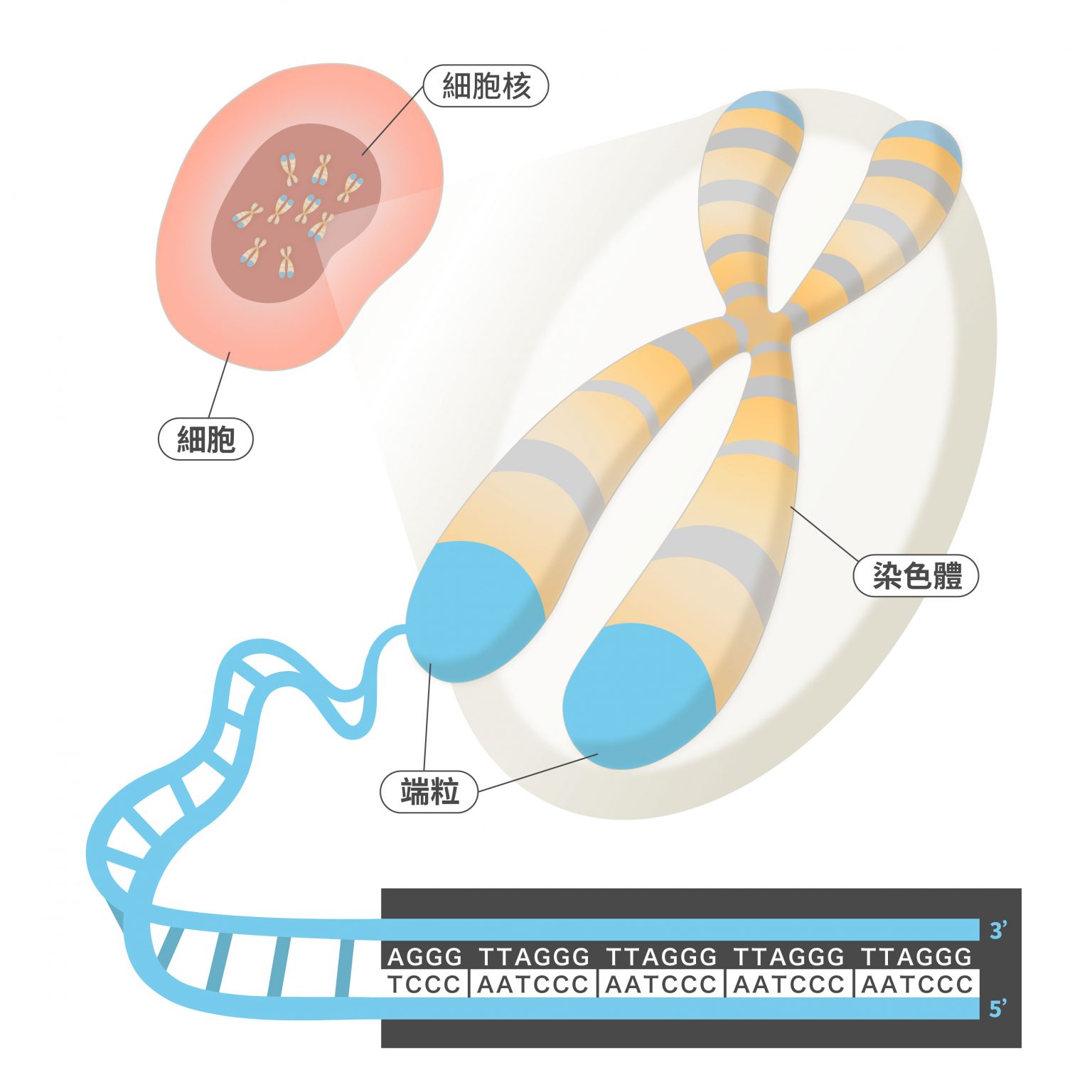
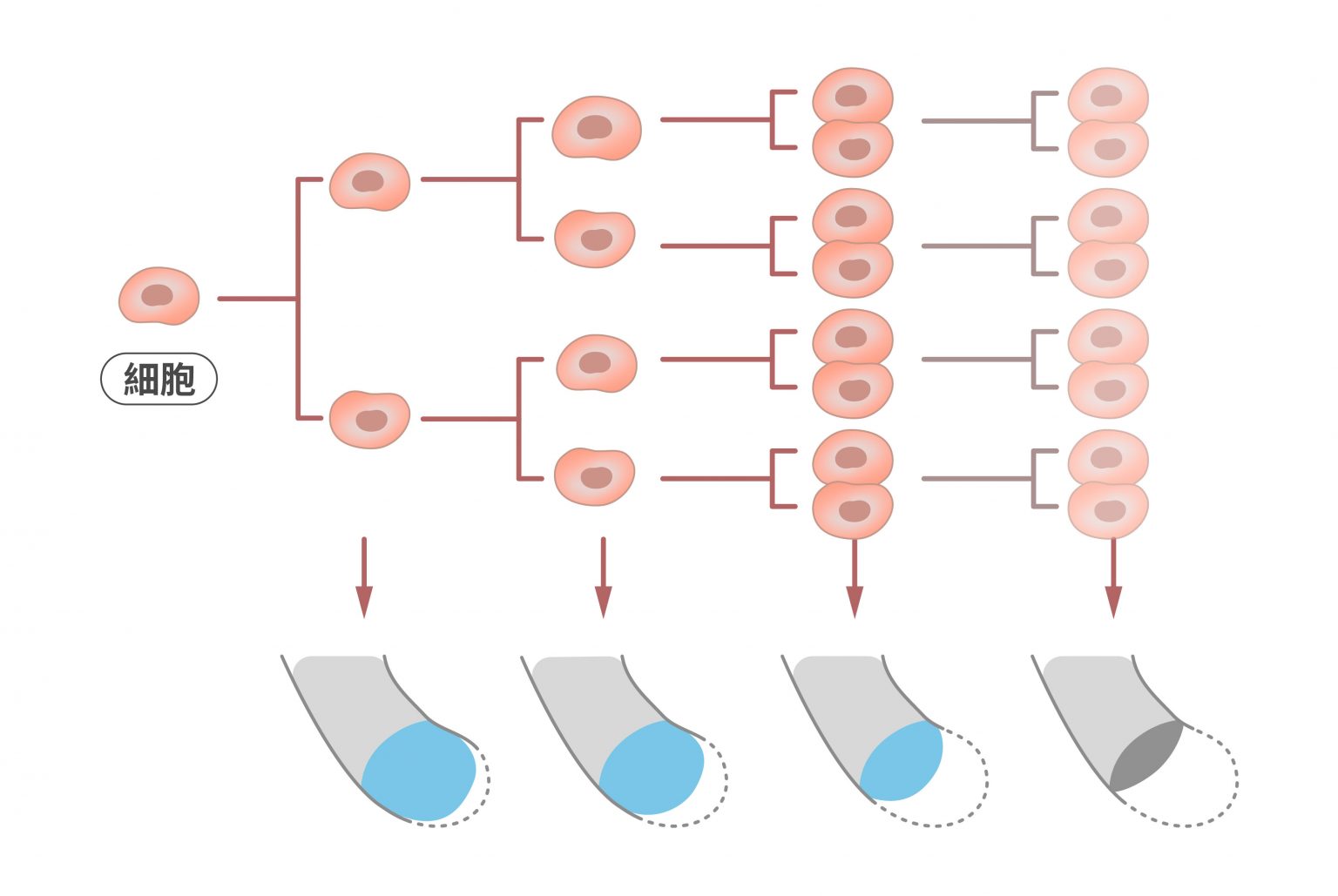
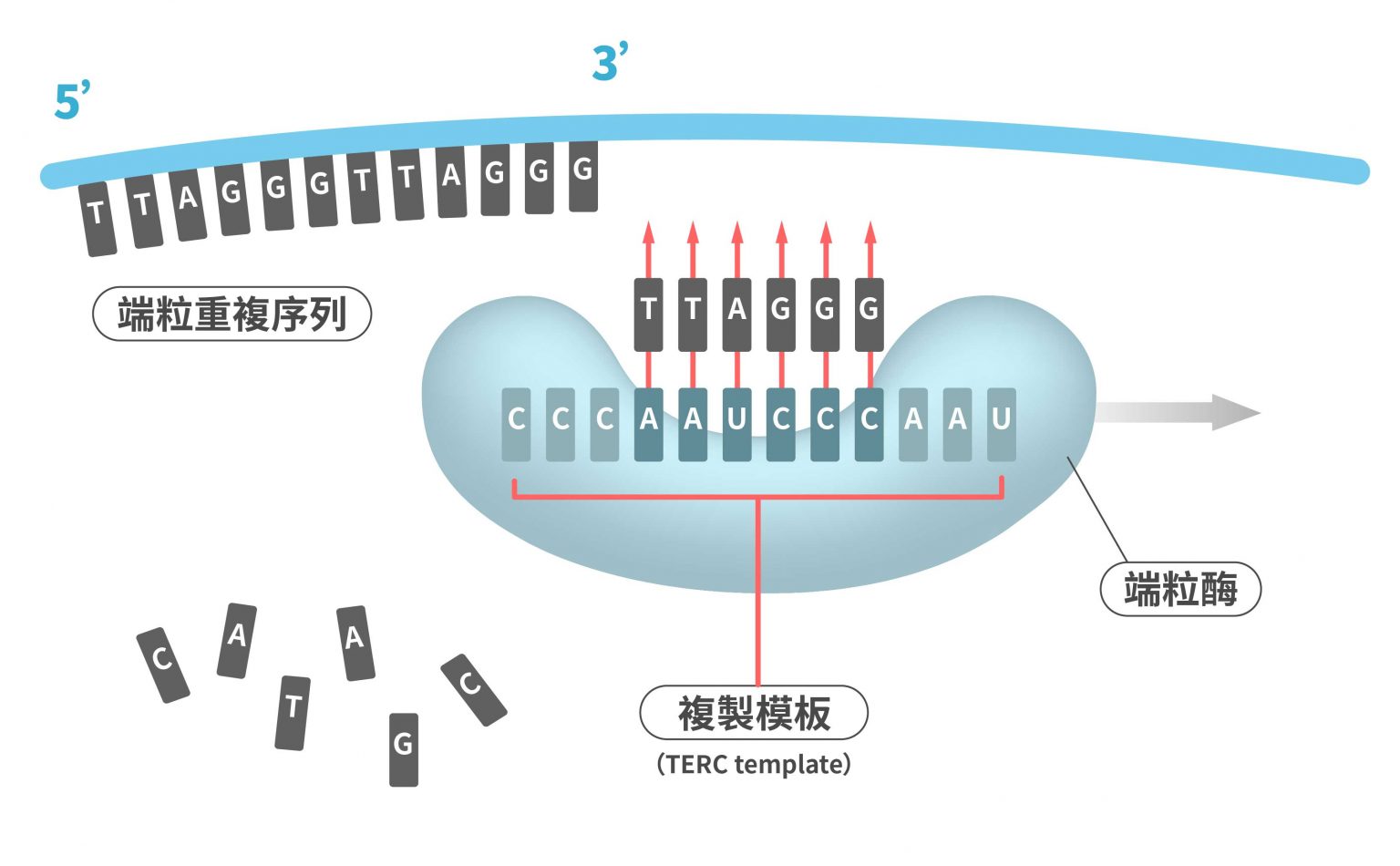
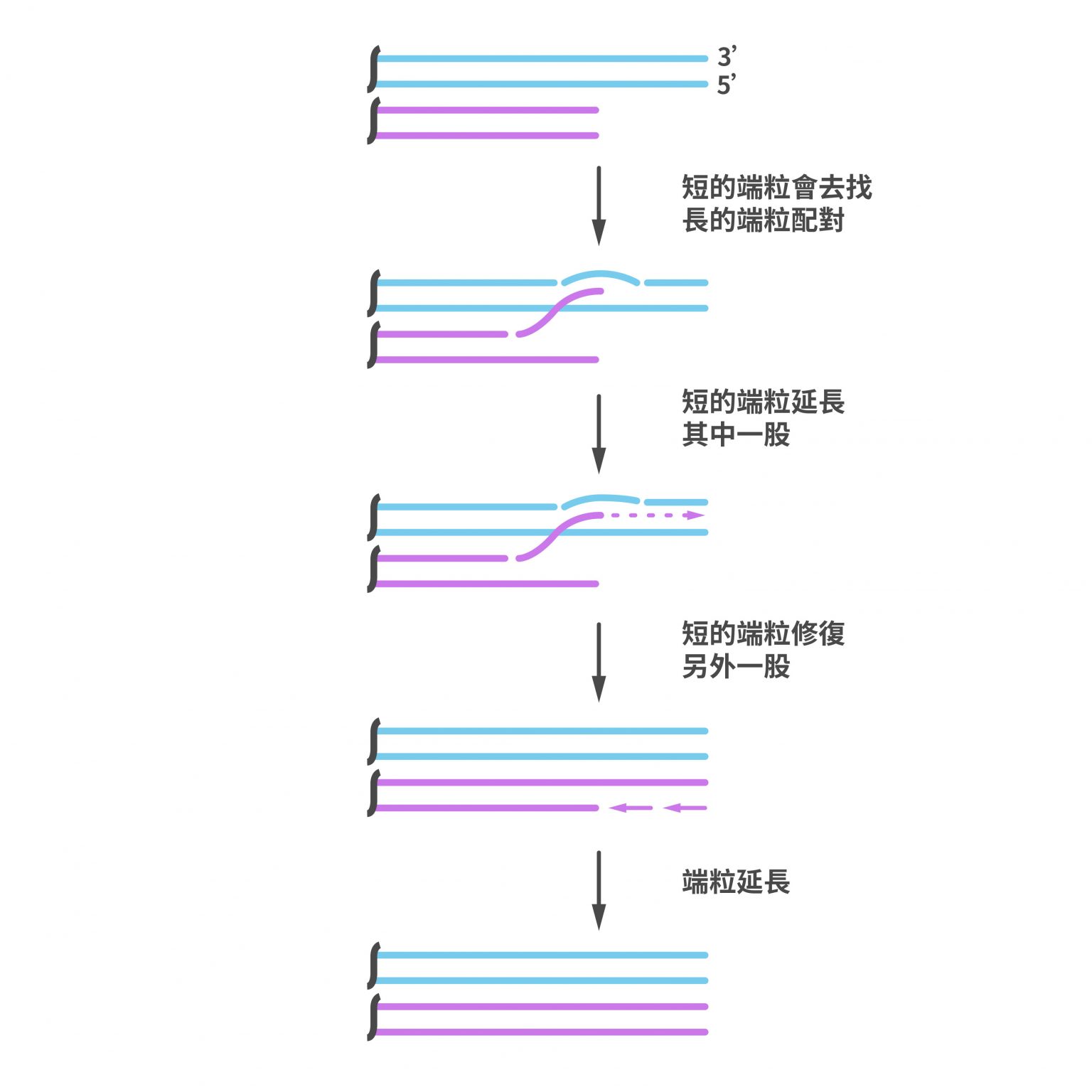
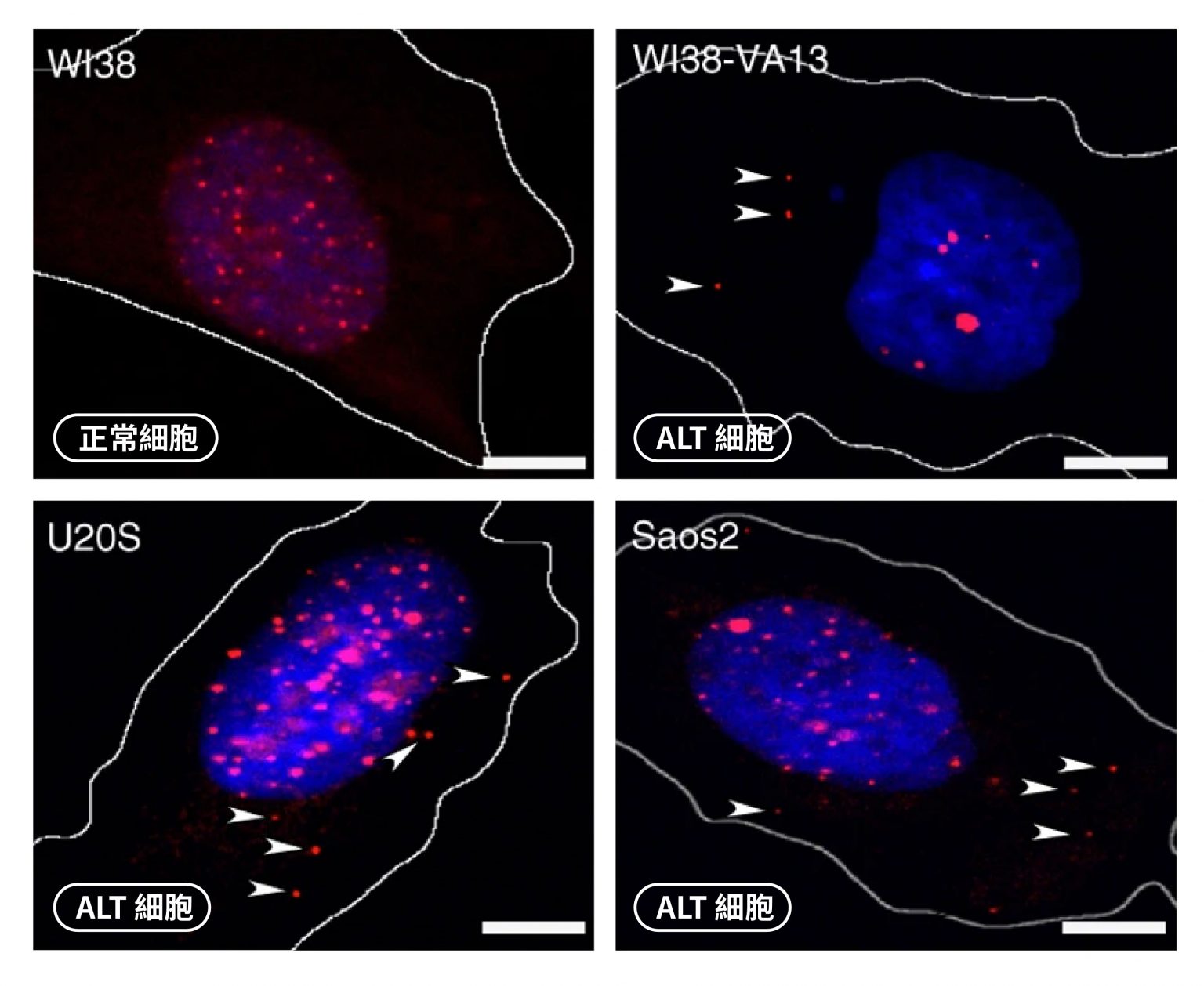
染色體端粒的消長,牽動細胞老化與癌細胞發展,對於人的壽命有決定性影響力,端粒是當前人類健康與疾病的重要研究主題。陳律佑與他的研究團隊致力於端粒研究,揭開了 ALT 癌細胞如何逃避免疫機制的秘密,在「研之有物」之前的文章〈解密兒童癌症:ALT 癌細胞如何延長端粒、逃避免疫系統?〉有詳細討論,以下簡述研究內容。
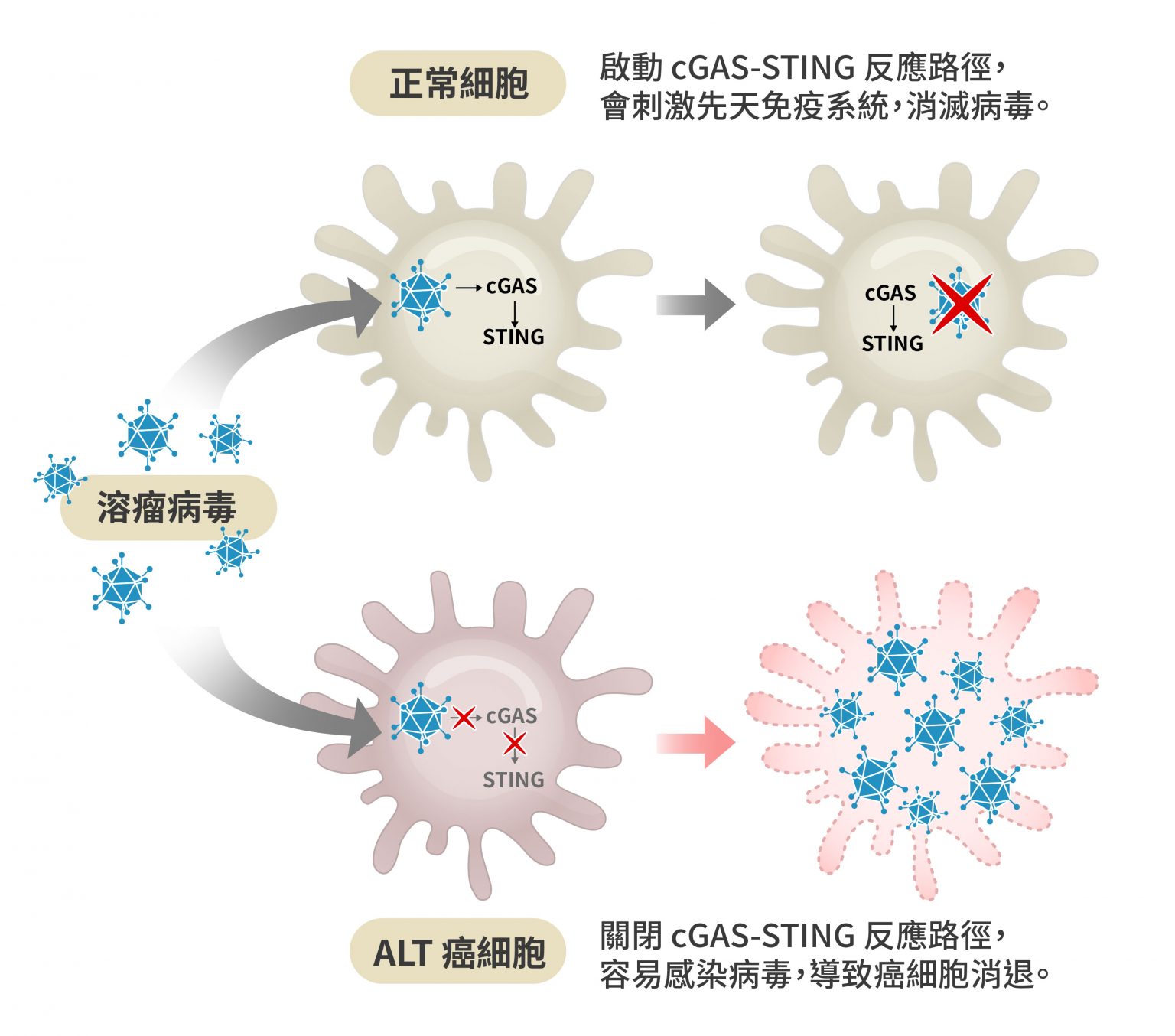
首先是確認 ECTR DNA 會開啟 cGAS-STING 感知路徑,激發人體先天免疫反應;接著發現 ALT 癌細胞會讓 STING 蛋白消失,使 cGAS-STING 路徑失去作用,免疫機制無法啟動,癌細胞才能夠生生不息;目前,研究團隊正在積極尋找治療 ALT 癌症的潛在方法。
陳律佑的研究成果,不僅推進了端粒基礎研究,還與和信治癌中心醫院的陳榮隆醫師合作,結合學術研究與臨床醫療,在兒童罕病治療扮演重要角色。不過,擅長研究端粒的陳律佑,並非一開始就進到生命科學領域,他在求學時期也經歷了一段自我探索的過程。

唸的是化學 卻成功在生科找到自己的歸屬
「我高中其實沒有唸過生物,當時對化學比較有興趣。」陳律佑笑著說,依著高中時的興趣,陳律佑進到清華大學化學系。但是讀著讀著,他逐漸發覺所學內容似乎跟自己想像的不大一樣,於是陳律佑開始到各系所修課,接觸不同領域的知識。
他到物理系、數學系的課堂學習,也去修生命科學系的課,生科成功喚起陳律佑的興趣。「細胞生物學、分子生物學、遺傳學等等,這些課程內容就發生在我們身體,與生活息息相關,實在非常吸引我。」陳律佑說。就讀化學系的他不僅修完生命科學系的必修課,還主動去修實驗課,更進入細胞生物學實驗室裡面研究專題,就讀生命科學系碩士。
剛開始他是研究細胞的熱休克反應。「研究熱休克的方法,簡單來說就是燙一下細胞,然後觀察細胞的反應。」陳律佑解釋,溫度上升 5 度,就會讓細胞內化學反應發生錯亂,熱休克蛋白會大量表現,可協助其細胞穩定蛋白結構,因應環境改變,維持細胞生理。
雖然陳律佑專題和碩士班都在研究「細胞熱休克反應」,但是他到美國攻讀博士時,決定挑戰全新的領域。「我覺得,自己碩士班到博士班這段時間,都還是持續地在自我探索。」陳律佑說。
博士班一年級期間,除了修課以外,還投入時間進入三個不同領域的實驗室實習,兩個是研究蛋白質結構、一個是研究老化生物學。最終陳律佑選擇了與過去研究截然不同的主題:老化生物學,也就是研究端粒的實驗室進行博士論文研究。
「碩班是研究細胞生物學,但當時我想要投入自己沒有接觸過的領域。」陳律佑說。首先他在結構生物學的實驗室待了一年,閱讀文獻、純化蛋白質結晶、分析蛋白質結構,一年下來也頗有進展。
只是,陳律佑發現分析結構跟自己想要的不太相符。「我對細胞生物學還是比較有興趣,因為每個實驗的結果都可以學習新的生物學,有新的發現。」陳律佑提到,即使指導教授對於他想換研究主題這件事也頗為訝異,他還是決定照著自己的直覺走,轉換到研究端粒的實驗室。於是,陳律佑從 2005 年開始投入端粒研究,一直持續到現在。
回想起當初的決定,陳律佑認為,選擇實驗室的時候,首先要考量自己的興趣。「每一個時刻,都可以去思考:這是不是我想要的、是不是真的喜歡?」陳律佑強調,如果無法肯定的回答,那可能就是還沒找到真的興趣與題目。第二考量就是實驗室的風格與自己個性是否合適。陳律佑提到,自己的個性比較開放,喜歡自由發揮,同樣的,在帶學生時也會給很大的自主空間,不過,往往個性獨立的學生比較能夠適應這種方式。

有別於「美式」實驗室 到瑞士體驗獨特的「歐式」風格
結束博士班階段,陳律佑再度展開全新的研究旅程。原先他博士後研究曾考慮兩個實驗室,一個在美國史丹佛,另一個是位在瑞士洛桑的瑞士理工學院,陳律佑選擇了後者。「我會去瑞士,是因為我喜歡他們的端粒題目,這實驗室的端粒酶生化實驗技術是全世界最好的。」陳律佑笑著說。也因為從美國換到歐洲做研究,讓他見識到,世界上有別於美國的另一種實驗室。
「臺灣科學研究其實滿美式的,當初從臺灣到美國,我會覺得美國就是更進步、放大版的臺灣。」陳律佑說。美國地大物博,學術資源豐富,但研究氛圍跟臺灣很像,一樣是鼓勵埋頭努力工作,提倡競爭的精神。
位在歐洲的瑞士卻是截然不同的世界。「從美國德州到瑞士洛桑後,突然間什麼東西都縮小了,路上不見皮卡而盡是小車,更沒有 Costco 大量販店,換成了小超市,餐館,還有市集。」陳律佑提到,除了建築景物,研究的習慣也大相徑庭。一開始以為瑞士人比較悠閒、慵懶,但實際觀察後發現,其實他們做事非常有效率。
「不論是研究還是行政工作,都有建立完整的系統,讓大家能夠很有效率地處理事情。」陳律佑指出,因為做事有效率,所以工作日也會有許多時間可以喝咖啡聊天,而且沒有人會在晚上或週末到研究室加班。實驗室除了瑞士人,還有來自義大利、德國、法國、東歐……的人,聊天的內容除了實驗內容或科學新知,也可以是生活經驗。透過交流與腦力激盪,研究人員常常會有自發性的合作,也會靈光乍現,有新的創意想法。
瑞士國土比臺灣大一些,人口只有 800 多萬,大約是臺灣的三分之一多一些,但是瑞士諾貝爾獎獲獎人數卻有將近 30 位,遠多過臺灣。陳律佑認為,強調做事高效率,以及實驗室之間一起喝咖啡交流的「閒聊文化」,絕對是關鍵之一。
瑞士跟美國相比,國土、人才跟資源都有相當大的差距。美國資源多,況且美國實驗室裡,來自亞洲國家的學生與研究人員都還特別認真埋頭工作;而瑞士學術界是把有限的時間跟資源做到最有效率的使用,空出來的時間則用來休息、好好陪伴家人,這方面是值得臺灣思考的。
除此之外,歐洲實驗室裡的指導風格也不太一樣。「在美國,實驗室的指導教授會被稱為 Boss;而在瑞士,我的指導教授卻像是 Advisor 。」陳律佑解釋,會被稱作 Boss 是因為美國的指導教授比較像是老闆、頂頭上司的角色,學生做的研究題目通常會是指導教授大計畫中的一小部分或是子計畫。
在瑞士的話,指導教授比較像是同事、顧問,學生或博士後對自己的研究都很有想法與主見,有疑問可以向指導教授請教討論。在瑞士實驗室做研究的自主性、自由度高,有興趣的人做著自己喜歡的題目,才會有更多動力來發揮創意。陳律佑於瑞士完成博士後研究,2013 年底就進到中研院。

一通電話 開啟臨床合作的新頁
目前陳律佑除了在中研院做基礎端粒生物學的研究,同時也與和信治癌中心醫院陳榮隆醫師合作,為患有端粒疾病的病人提供學術支援。談到他與臨床合作的開端,原來是一通請求協助的電話。
有天他接到一位病患家長的電話,「家長說小朋友被診斷出可能有遺傳疾病,想請我協助判斷是不是端粒相關的基因變異。」陳律佑說到,回想起當時情況,那位小朋友先在和信醫院,由陳榮隆醫師診斷出重度再生不良性貧血,但其他異常狀況也讓陳醫生懷疑可能有端粒功能缺陷的因素存在,於是家長想到要向國內研究的權威機構中研院來尋求協助。
陳律佑與實驗室團隊鑑定之後,確認端粒缺陷,也找到導致疾病的變異基因,證實病童的確患有端粒遺傳疾病,因此他得以接受特殊方式進行骨髓移植手術。「雖然他是造血功能有問題,但因為原因出在端粒身上,無法藉由一般標準的骨髓移植治療。」陳律佑解釋。
研究團隊與醫療機構合作,讓一位罕見疾病的兒童獲得醫治,這讓陳律佑留下深刻的印象。「之前都是做研究然後發表論文,但我第一次感受到,原來我們的研究工作確實可以直接幫助他人。」陳律佑表示,這次經驗對他來說意義非凡。
雖然成功移植骨髓解決造血問題,令人遺憾的是,三年之後病童還是因肺臟功能喪失而不幸離世。陳律佑提到,當時他們確認是端粒疾病,也找出合適的療法、解決造血系統的問題,然而病童全身細胞的端粒都有缺陷,還有很多問題並沒有得到解決。「對我而言,這又是另一個衝擊:原來我們的研究其實相當有侷限。」陳律佑說。
這也給陳律佑帶來一些啟發。他提到:「對我來說,做研究就是為了要解決問題。而這次的經驗,讓我思考如何將基礎端粒生物學的研究,更進一步導向與疾病相關的課題,期望未來的研究成果,有機會能為民眾解決問題。」
之後,陳律佑與和信治癌中心醫院的陳榮隆醫師保持著緊密合作。每當陳榮隆在臨床上碰到棘手的病例,就會聯繫陳律佑,一起尋找疾病的源頭。
「因為兒童罕見疾病個案不多,一年就幾個,除非是大型醫療機構,不然無法投入穩定資源。」陳律佑解釋,兒童罕見疾病在診斷或治療上,往往不易獲足夠的醫療資源,秉持著回饋社會的初衷,實驗室就盡量提供協助。
「中研院的研究資源相對豐富,所以在能力許可之下,我們會協助端粒疾病方面的鑑定。」陳律佑說,一開始他是自己撥出實驗室的研究能量來協助病童。行善的人不孤單,幾年之後,陳榮隆接觸到的病童家長們,便成立了「台灣重症兒童協會」,讓臨床治療與研究端能夠執行一系列計畫,為更多患者服務。

為罕病建立基因資料庫
在協會支持之下,陳律佑與陳榮隆結合中研院研究資源與和信治癌中心醫院臨床醫療,開啟了「重症基因庫暨細胞/藥物研發」計畫,為的就是照顧更多的兒童癌症患者。計畫分為幾個部分:建立重症病人基因變異資料庫、製備特異性免疫細胞,以及精準化藥物治療與規劃。
首先要建立資料庫:一個症狀出現背後有非常多可能性,當患者來尋求醫療協助時,第一件要做的事情就是「檢查」,找出身體問題,了解生病原因。「兒童罕見疾病五花八門,我們從基因下手,先把患者的基因全部定序,然後跟一般人比對,找出可能導致疾病的『突變點』。」陳律佑說。
研究端建立病人的基因變異資料、找出致病突變,作為臨床診斷和治療的參考與指引。
另外,資料庫的資訊也會用來協助製備特異性免疫細胞。「簡單說,特異性免疫細胞就是被訓練好,專門對付某個特定目標的免疫細胞。」陳律佑解釋,以兒童癌症為例,就是把免疫細胞拿到體外,教會它認識癌細胞後,再增加數量、放回病人身體內,讓這些免疫細胞去消滅癌細胞。
除了跟和信治癌中心醫院合作之外,高雄醫學大學的團隊也有加入計畫,負責規劃患者用藥的部分。「治療疾病時,用藥是很重要的一個環節。」陳律佑指出,要用什麼藥物、要用多少劑量,就由高雄醫學大學團隊以藥物動力學來監測。透過建立基因庫,將設計特異性免疫細胞,還有精準的藥物治療方法,期待未來能提高兒童癌症重症治癒率,同時降低併發症或副作用。
建立平台、完善系統,讓研究有溫度、與社會連結
跟醫院的跨機構合作計畫所蒐集到的患者檢體與疾病資料,會經由實驗室定序、找出「突變點」,並且分析基因突變與疾病之間的關聯。不過,即使找出問題的可能關鍵,也不能直接在病人身上做實驗,所以都需要回歸到實驗室先從細胞或動物測試做起。
建立完善體外實驗系統是陳律佑接下來的課題。「我們想要建立一些平台,來進行體外細胞、以及動物的 ALT 癌症實驗。」他說。因為研究已經揭發 ALT 癌細胞逃離免疫系統的招數,之後如果想要做一些藥物測試,或是嘗試修復被中斷的 cGAS-STING 感知路徑,以找出消滅癌細胞的方法,這些工作都需要倚賴體外細胞或動物實驗系統的建立。
不論是 ALT 癌症,或其他端粒相關罕見疾病的研究,陳律佑的終極目標都是回饋社會、幫助有需要的患者。他認為,學者能夠無後顧之憂地埋頭做實驗,也是因為有國家、社會的資源支持,所以研究工作不是特權而是責任。
「研究不是只有發表文章、或自己開心就好,我想做的是跟大眾有關、『有溫度』的研究。」陳律佑笑著說。

延伸閱讀
- 陳律佑個人頁面
- 林承勳(2023)。〈解密兒童癌症:ALT 癌細胞如何延長端粒、逃避免疫系統?〉,《研之有物》。
- 陳榮隆(2022)。〈重症基因庫暨細胞藥物治療研發計畫〉,《和信醫訊》。