躲貓貓,又叫做捉迷藏,是大多數人的童年回憶,這個看似簡單的遊戲,事實上參與者需要一定程度的心智能力才能進行。在 2019 年 9 月的一篇科學文章中,一群科學家們發表了他們如何透過實驗,發現老鼠竟然也懂得玩捉迷藏,甚至看起來樂在其中。
看影片找靈感,玩捉迷藏發論文
德國洪堡大學(Humboldt university) 的神經科學家 Michael Brecht,某一天看了一則飼主跟寵物鼠玩捉迷藏的影片,這讓他開始好奇這個影片是否只是個誤會,又或者是老鼠真的會玩捉迷藏?
Brecht看的不是youtube,是科學。
於是他和團隊設計了一個 30 平方公尺大的房間,並且利用厚紙板和來製造遮蔽,放置了數個透明或不透明的盒子。他們一共製作了七個藏匿地點給老鼠,以及三個藏匿地點給學生 Reinhold。
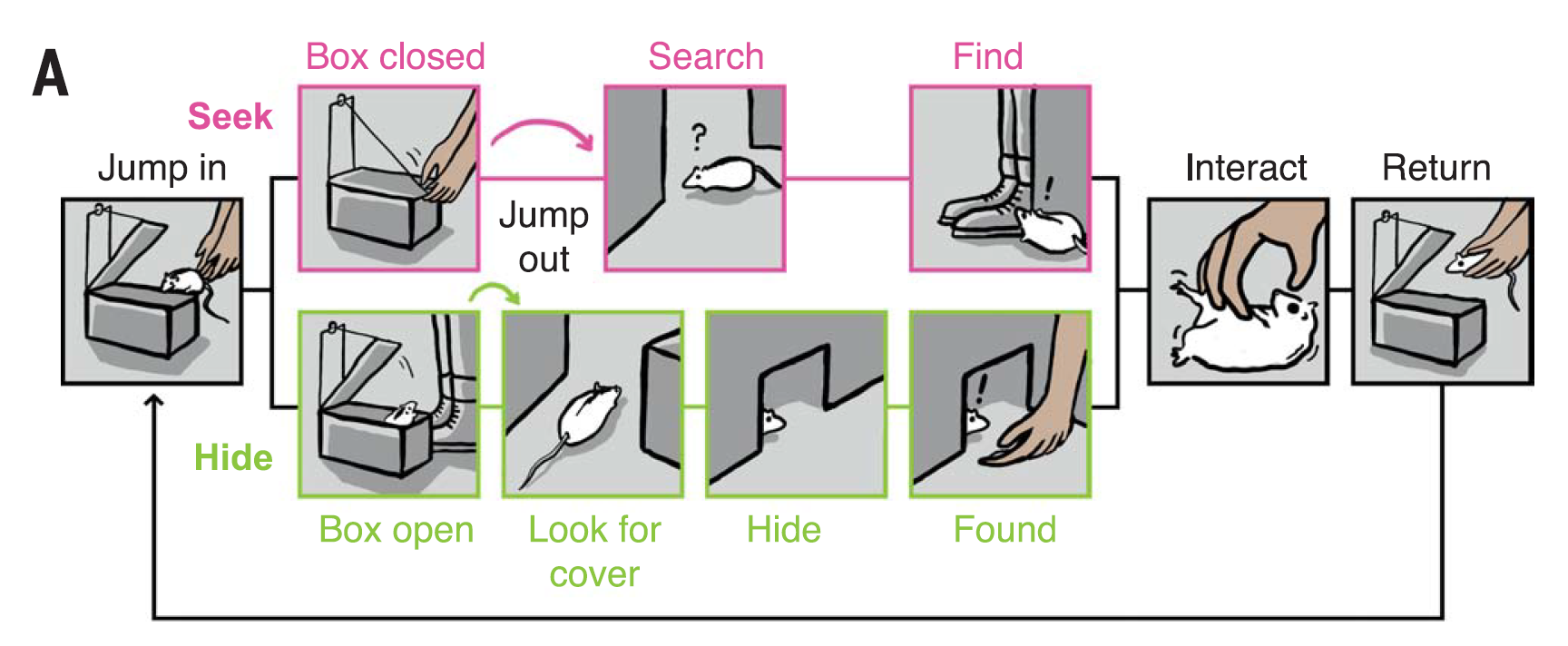
當老鼠當鬼時,Reinhold 會把老鼠放進盒子後蓋起來,接著跑去躲起來,再利用遙控器將蓋子打開。經過訓練後,老鼠開始知道蓋子打開是代表可以去尋找 Reinhold 的信號,當老鼠找到她之後便會收到獎勵。
老鼠當鬼尋找 Reinhold,找到後獲得獎勵
換 Reinhold 當鬼時,她會打開盒子並蹲在旁邊,等待老鼠跳出盒子並躲到藏匿處,老鼠被找到後一樣會獲得獎勵。和一般動物訓練不一樣的是,實驗中用搔癢和撫摸作為獎勵而非給予食物。
經過兩周的訓練,六隻老鼠中共有五隻學會玩捉迷藏,不會在遊戲途中混淆或變更角色。
為了瞭解老鼠在玩捉迷藏的狀態,他們在老鼠的腦中植入了可攜帶的裝置,在主導記憶學習的前額葉皮質區域,紀錄了 180 個神經元的電子訊號。當 Reinhold 關起盒蓋,提示老鼠誰要當鬼時,有大約三分之一的細胞開始產生訊號。Brecht 表示這些現象代表這些區域可能對於學習規則相當敏感。
不只會玩,老鼠還會為了娛樂而玩
除了對遊戲的基本認知的,實驗中有幾隻老鼠甚至表現出意料外的能力,當 Reinhold 搜尋房間時,老鼠會偷偷移動到它已經看過的地點,彷彿它們推測這些地方不會再次被搜尋。另外在躲藏時,老鼠也更喜歡躲在不透明的盒子中並且保持安靜,好讓自己較不容易被發現。Brecht 認為這些行為都顯示老鼠有能力從其他生物的角度去思考,表示老鼠比想像中來得聰明。

而另一件令人好奇的是,老鼠玩遊戲是為了娛樂或是獎勵。
Brecht指出實驗中老鼠有好幾個行為都顯示它們是為了娛樂而玩,例如當老鼠發現研究者時,會展現出快樂的跳躍 (freudensprung)。這個動作在哺乳類動物中很常見,兔子、羊和人類都有類似的行為來表達開心。老鼠被發現後,也常常不接受獎勵,而是會跑去其他地點躲藏,似乎不想讓遊戲結束。(跟熬夜刷首勝的我有點像?)
我們與鼠的距離
這項研究最重要的貢獻是證明了老鼠具有足夠的心智能力,包括了決策、位置導航、理解規則和角色設定來進行捉迷藏遊戲。除了被搔癢會發笑2,為了夥伴可以放棄巧克力之外3,科學家又找到了我們之間新的共同點。
另外實驗其實還有第二階段,研究者要讓四隻以上的老鼠一起玩捉迷藏,進而觀察老鼠們的互動,看看是否會有更意外的行為出現,就讓我們一起拭目以待之後的結果吧。(好了快去報名搞笑諾貝爾獎。)
看完文章,你是否準備好想要和你的寵物進行一局 science 等級的實驗了呢?如果沒有寵物的話,也不要太難過,或許遊戲早就開始了,只是你不知道而已,吱吱! ψ(`∇´)ψ

參考資料
- Reinhold, A. S., Sanguinetti-Scheck, J. I., Hartmann, K., & Brecht, M. (2019). Behavioral and neural correlates of hide-and-seek in rats. Science, 365(6458), 1180-1183.
- Ishiyama, S., & Brecht, M. (2016). Neural correlates of ticklishness in the rat somatosensory cortex. Science, 354(6313), 757-760.
- Sato, N., Tan, L., Tate, K., & Okada, M. (2015). Rats demonstrate helping behavior toward a soaked conspecific. Animal cognition, 18(5), 1039-1047.