- 許嘉合/中央研究院/生物多樣性研究中心/博士後研究員
由目前的證據推測,科學家們認為這可能是因為神經系統在演化上出現的時間比後天免疫系統還早,在後天免疫系統還沒發展出來的年代,神經系統在動物演化的長河中就扮演了與細菌房客交流的重要的角色!
「靠!絞痛又開始了,而且一陣比一陣還痛!」心裡忍不住的罵了髒話後,我還是認命的吞下ㄧ顆止痛藥。對許多受原發性經痛困擾的女性朋友來說,止痛藥才是我們的好朋友。真不知道痛覺神經演化出來折磨人幹麻?其實,這一切的始作俑者就讓我們怪罪給水螅與它的祖先!
水螅 (hydra) 生活在淡水中[註1], 屬於刺絲胞動物門 (Cnidaria)、水螅蟲綱 (Hydrozoa)。同樣隸屬於刺絲胞動物門的還有水母、海葵、珊瑚。它們擁有簡單的散漫神經系[註2],是第一群具有神經系統的動物。其中水螅因為構造簡單,培養、繁殖容易的特性,最適合拿來當模式物種來研究神經傳導。
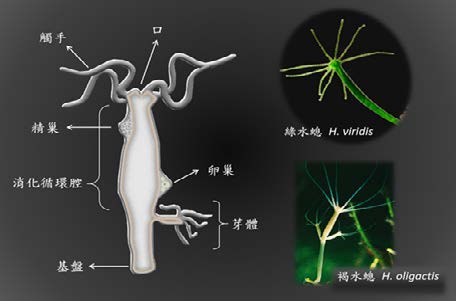
- [註1]:水螅構造簡單,呈輻射對稱:觸手環繞在口部周圍用以捕食;基盤用來附著或移動。雌雄同體,有精巢和卵巢可行有性生殖,但通常行無性的出芽生殖。常見的種類有綠水螅與褐水螅。
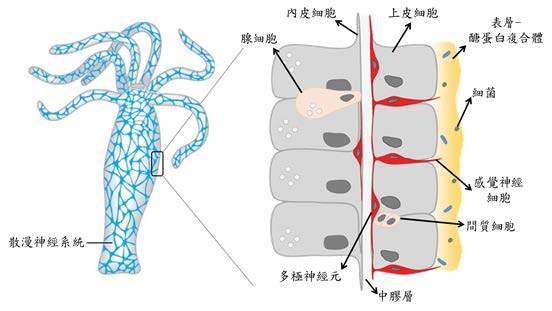
- [註2]:水螅擁有最簡單的散漫神經系統,神經系統缺乏統整訊息的中樞,具有兩種不同的神經細胞,包括感覺細胞 (sensorycells) 與多極神經元 (ganglionneurons)。水螅上皮細胞表層的黏膜主要成分為醣蛋白複合物,適合細菌居住。
神經系統的功能與定義一直都被認為是清晰無疑的:它可以接收環境中的物理、化學訊息,讓生物能感知、並能對這些訊息有所反應或行動。然而近年來科學家發現神經系統在演化初期可能具有不同功能,可能被用來與周遭環境中的微生物溝通,還能控制微生物菌相的組成。疑!這聽起來是不是很像後天免疫系統的工作內容?由目前的證據推測,科學家們認為這可能是因為神經系統在演化上出現的時間比後天免疫系統還早,在後天免疫系統還沒發展出來的年代,神經系統在動物演化的長河中就扮演了與細菌房客交流的重要的角色!
不會說話的水螅房東,如何和他的細菌房客溝通?
然而,水螅到底是怎麼利用神經系統來跟它們的細菌房客溝通的呢?在水螅 Hydra magnipapillata 的上皮細胞 (epithelialcell) 表面,有群細菌定居在那。裡面數量最多(佔了 75% 以上)的成員是 β- 變形菌綱(β-Proteobacteria)的成員,尤其是曲桿菌屬 (Curvibacter) 的菌種。第二多和第三多的居民則是 γ- 變形菌綱 (γ-Proteobacteria) 和擬桿菌門 (Bacteroidetes) 的菌種。
細菌房客的種類組成會受水螅房東的種類和健康狀況影響,並且會受水螅上皮細胞分泌的抗微生物胜肽 (antimicrobialpeptides) 抑制。然而,抗微生物胜肽的生成又會受到神經系統的抑制(圖3,a)。因此,科學家在缺乏神經系統的水螅突變個體上,發現過量的抗微生物胜肽導致上皮細胞原有的 β- 變形菌綱菌種大量減少到只剩下原本的一成。但是原來的第三名擬桿菌門菌種的數量則增加了十倍。所以雖然社區裡面的總菌口數還是維持不變,但組成卻大大的改變了。
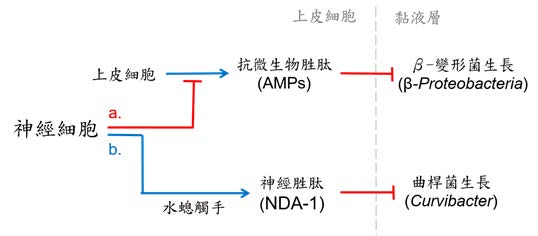
除此之外, 神經細胞還會分泌另一種叫做 NDA-1 神經胜肽 (cationic neuropeptie), 去控制主要細菌居民曲桿菌 (Curvibacter) 在自己身體上的分佈位置!這種神經胜肽 NDA-1 在水螅的觸手細胞製造得比較多,合成後會被傳送至上皮細胞表面的黏液層中,用來抑制曲桿菌生長(圖3,b)。這也是為什麼曲桿菌主要出現在水螅的軀幹而非觸手上的原因。這個結果證實水螅能用神經系統控制細菌社區的成員組成與分布位置。
垃圾吃垃圾大?長細菌的水螅好壯壯?
但是,如果你以為細菌只能單方面受制於水螅,那就錯了!細菌與水螅的溝通是雙向的。雖然目前還沒有直接的證據,可是當研究人員用抗生素去除掉水螅身上的細菌後,發現如果水螅身上沒有細菌的話,身體收縮的頻率會不正常升高。另外在水螅胚胎發育的過程中,如果和有正常菌陪伴成長的水螅胚胎相比,無菌的水螅胚胎在發育時更容易發生嚴重的真菌感染。所以,好房客細菌可以保庇你健康長大!而為了要讓好房客細菌乖乖的、不離家出走、不失控,神經系統可是擔負著重要的使命呢!
整合目前在水螅的研究結果,科學家推測神經系統不但可以偵測環境中的細菌、辨認出其中的特定菌種,還可以依據細菌房客組成的不同,來調節體內的生理代謝狀況或控制、篩選體表菌相的組成。當有房客搗亂時,它們還可以引發上皮細胞的先天免疫反應,來維持秩序。
當研究回到人身上,有腦的我們也能和細菌溝通嗎?
藉由研究模範房東水螅與細菌房客的對話,我們才有機會進一步瞭解神經、免疫系統與共棲微生物的交互作用。例如水螅上的共棲菌如何影響神經系統的放電,以及如何影響水螅的行為。這樣的研究對應到人類,就和最近很夯的:腸腦軸線 (gut-brain axis) 有關。所謂的「腦腸軸線」,是指腸與腦兩個器官間有神經網路讓彼此,連結溝通。近年來科學家發現,藉由這條專線,腸內的菌群可以影響大腦的發育、功能與內分泌系統;而大腦也利用這條熱線控制腸胃道內的內分泌與免疫反應,進而影響了腸道內的菌群組成。
所以當你緊張時可能會拉肚子或引起腸躁症;而當你飲食不正常造成腸內菌相失衡時,也可能引起過敏反應或增加焦慮、憂鬱行為。廣義來說,腦腸軸線其實包含了腸道菌群、神經系統、內分泌系統與免疫系統。其研究範疇更可以橫跨微生物學、生理學與神經心理學,在高等生物上所牽涉到的反應非常的錯綜複雜。因此,或許藉由研究小巧簡單的神經模式物種-水螅,能夠幫助我們釐清一些蛛絲馬跡,找到新的答案。
在了解了神經系統的重要性與在演化中所扮演的角色後,我比較能體諒神經系統這一路走來所負擔的工作既複雜又辛苦。我想下次經痛時,我我我….. 髒話會少罵一點的!
參考資料
- Augustin R, Schröder K, Murillo Rincón AP, Fraune S, Anton-Erxleben F, Herbst E-M et al. (2017). A secreted antibacterial neuropeptideshapes the microbiome of Hydra. Nature Communications 8: 698.
- Bosch TCG, Miller DJ (2016). The hydra holobiont: a tale of several symbiotic lineages. In: Bosch TCG, Miller DJ (eds). The Holobiont Imperative: Perspectives from Early Emerging Animals. Springer Vienna: Vienna. pp 79-97.
- Murillo-Rincon AP, Klimovich A, Pemoller E, Taubenheim J, Mortzfeld B, Augustin R et al. (2017). Spontaneous body contractions are modulated by the microbiome of Hydra. Sci Rep 7: 15937.
- Reece JB, Urry LA, Cain ML, Wasserman SA, Minorsky PV, Jackson RB (2010). Campbell Biology, 9th edition. Pearson Education.
- Foster JA, McVey Neufeld KA (2013). Gut–brain axis: how the microbiome influences anxiety and depression. Trends Neurosci 36: 305-
312.

歡迎訂閱微雜誌MiTalkzine,加入 MiTalker 的行列,一起來認識這個星球上千萬種各式各樣的微生物吧!



































