- 作者/王惠瑜
基因編輯CRISPR技術的專利戰爭,開打
基因工程技術重大的發明-基因編輯技術(Clustered Regularly Interspaced Short Palindromic Repeats;簡稱 CRISPR),是一項如同神之手般切割基因的技術,在體外將有問題的基因進行剪斷後再補上正常的基因,讓遺傳性疾病治療成為可能,在技術應用的層面也非常廣泛,此項技術除了潛在的龐大商業利益外,更具備角逐諾貝爾獎的可能性,因此,浮上枱面的專利已開始點燃了競爭的序曲。

專利爭執的核心在於取得基因編輯 CRISPR 技術的時間點,加州大學珍妮佛.道娜 (Jennifer Doudna) 於 2012 年發表基因編輯技術 CRISPR 技術,並申請了相關的專利;而哈佛大學與麻省理工學院的張鋒研究團隊則申請 CRISPR/Cas9 技術應用在真核細胞專利,並採取「加速審查 (Accelerated Examination)」程序,在 12 個月內加速進行審查發明的可專利性,所以僅花 6 個月就取得了專利權。
但因兩造在專利申請時間相近、專利範圍相似,珍妮佛.道娜團隊在 2016 年向美國專利商標局申請專利衝突 (interference) 程序,要求撤回張鋒團隊的專利權利,美國專利商標局於 2017 年 2 月的判決指出,兩造申請的專利技術內容存在差異性,並且無法確認在張鋒之前有 CRISPR 技術用於真核細胞的研究,因此,雙方在 CRISPR 技術上並不重疊與衝突,所以判定張鋒團隊能保留其專利並擁有專利權。
技術競爭的原由除了來自於潛在的龐大商機利益的可能性外,還有研究學者所追求的至高榮譽諾貝爾桂冠,所以,兩造已在枱面上的專利互相競爭,本研究則以雙方的專利申請策略及專利布局來微觀枱面下的競爭態勢。
申請專利,雙方策略大不同
美國自 2013 年 3 月起實施 AIA 法案後,專利從先發明制改為先申請制,因此,專利申請日成為技術先後重要參考指標,本研究以美國專利商標局資料,檢索以張鋒及珍妮佛.道娜為發明人之專利,時間至 2017 年 8 月 30 日止。
從兩造的專利數量上比較,張鋒的 MIT 團隊(71 筆)在數量上是多於珍妮佛.道娜的 UC 團隊(42 筆),另外從競爭的起始年(2012)為基準,珍妮佛.道娜在 2012 年之前起就已開始陸續申請專利,但在之前張鋒是並没有專利申請的,在 2012 年之後才見積極申請專利,反觀珍妮佛.道娜在 2015 年張鋒獲證專利後,專利申請的數量才比較多,見(圖1)。
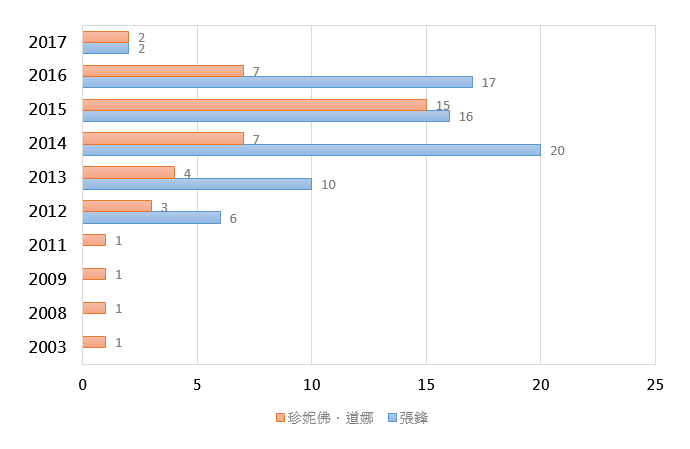
從以上的(圖1)得知,從數量上做比較,張鋒是較具有優勢的,但從專利的獲證、審查中、放棄等不同的法律狀態來分析真正有效用的專利,判斷技術受保護的真實狀態,實際上是否具有法律權利的保護。
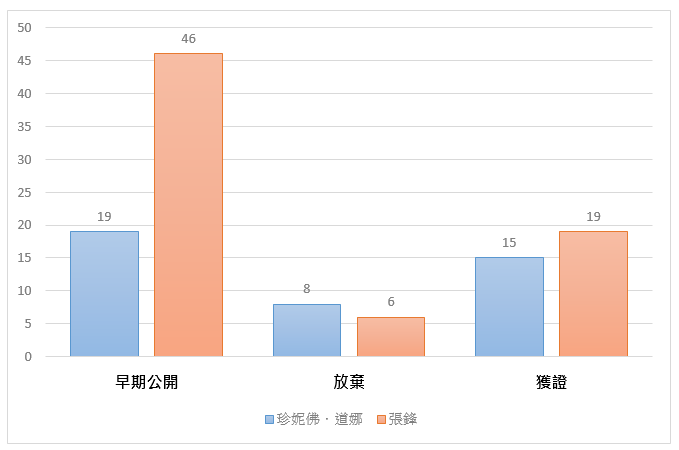
(圖2)是兩造專利有效性分析,從獲證專利數比較,張鋒已獲證的專利數量(19 筆)多於珍妮佛.道娜(15 筆);從兩造放棄的專利數量比較,珍妮佛.道娜在放棄專利數是略多於張鋒的;最後,比較兩造目前仍在早期公開中的專利,在審查當中而未來可能獲得的專利,張鋒目前在審查中的專利數量是遠多於珍妮佛.道娜。
從專利申請的數量分析發現,以張鋒所代表的 MIT 研究團隊,是非常積極在進行技術保護的,反映在專利申請時,多數專利都會運用快速審查的機制,其中又以系爭專利 (US8697359),從申請到獲證只花了短短 6 個月時間就快速取得專利,顯而易見的張鋒團隊在專利申請策略著重在快速獲得專利;另外在研究中也發現,珍妮佛.道娜在專利申請之後再放棄的比例明顯高於張鋒。
策略解盤:數量v.s網絡連結,誰具有優勢?
專利布局在專利申請時就已形成,美國專利法 111 及 119 條及美國專利審查指南 (Manual of Patent Examining Procedure) 指出,運用臨時申請案(Provisional Application,簡稱 PA 案)與第一次提出正式申請案的專利申請,皆可享有專利優先權(簡稱母案)。
若以原發明持續研究,在法定的期限內,延續先前所提出的專利申請為延續申請案 (Continuation Application;CA)、部分延續申請案 (Continuation-in-part Application;CIP)、分割案 (Division Application;DA) 等形式的專利申請案則皆為子案;以優先權號碼,將母案與子案之間的技術串起關連性,由不同的子案申請案策略進一步將母案未涵蓋的技術特徵逐步擴張原有保護範圍,將專利布局的範圍推展至深且廣。
本研究的專利布局研究,以兩造的專利申請,從美國專利商標局 PAIR系統的資訊整理繪製專利網,研究雙方專利國內優先權中母案與子案之間的關係,分別繪出珍妮佛.道娜專利布局(圖3)和張鋒專利布局(圖4);釐清雙方專利布局的脈絡重點,並分析兩造在專利布局的廣度與深度。
從研究中發現雙方共同的申請策略,皆利用臨時申請案取得較早優先權日期後,並在一年之內提出正式的專利申請案,因此,在每一個相同母案的技術群組內的專利,都有其技術相關性及延續性。
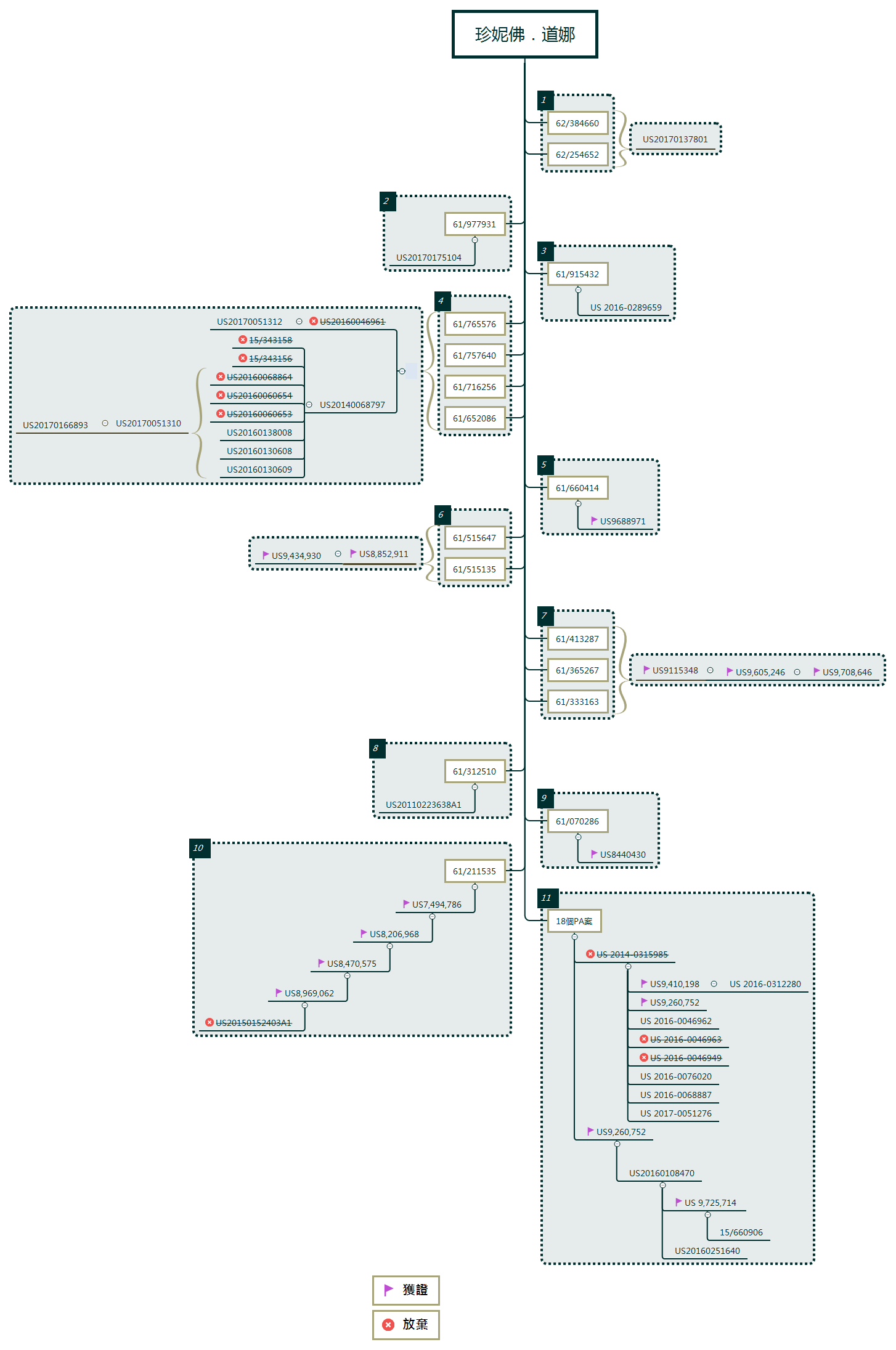
(圖3)為珍妮佛.道娜的專利布局,其專利數量雖少於張鋒,以多個臨時申請案合併為一個正式專利申請案,有 11 個技術群組合,顯示其專利布局具有技術多樣性,並且在同一母案中專利有階層的接續性,布局往下展開,其技術具有延續性,顯示專利網逐漸形成,又以技術群組 4、10、11 為重點的技術群,其中又以技術群組 11 為 18 個臨時申請案所組成,且為近幾年申請的重點技術群。
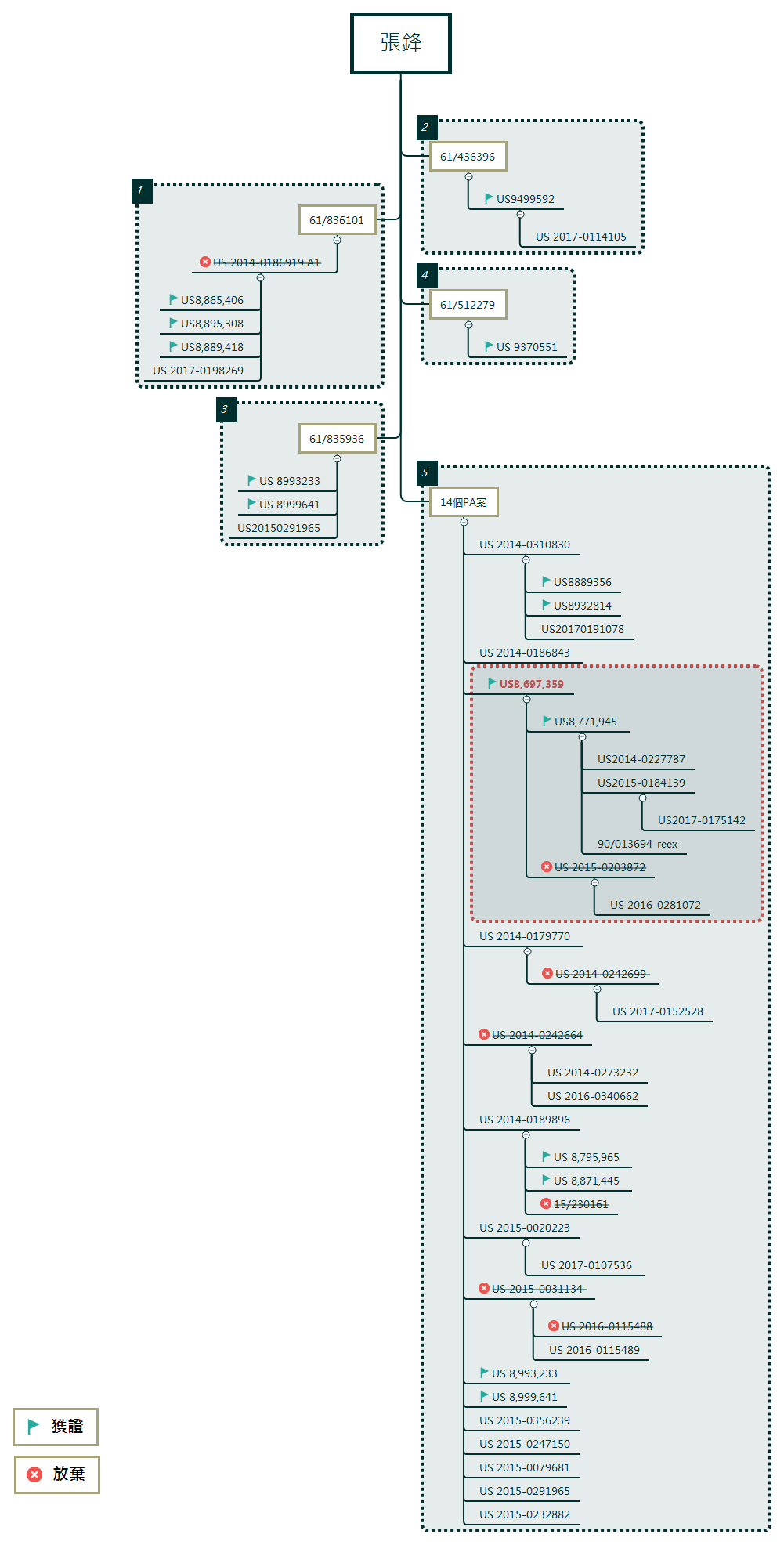
(圖4)為張鋒的專利布局,在專利申請及有效性的分析當中,張鋒在專利的數量上都具有顯著的優勢,但在專利布局上與珍妮佛.道娜的布局有明顯的差異,在前期皆以單一母案申請不同子案的策略(技術群組 1-4),為一個母案以不同技術特徵申請後續子案專利,在申請的策略上缺少階層性的展開,技術的延續性較為不足;專利布局的重點在技術群組 5,由 14 個臨時申請案所組成,為關鍵的技術群,展開成 15 支的技術群,成為具有廣度的布局後再各自往下展開,具有技術延續性,正逐步形成專利網中,其中又以關鍵專利 US8697359 最為重點布局,在往下分成二支後,並各自向下延續申請,詳見(圖4)的紅框。
不論結果如何,道德仍為最高原則
CRISPR 基因編輯技術所涉及的疾病診斷與治療,包含所需工具、套組、試劑、儀器以及相關藥物與處理等研究,讓 CRISPR 技術持續向前邁進,透過珍妮佛.道娜和張鋒等生醫學者的專利競爭,雙方在專利布局上步步為營,將重要的技術特徵運用臨時申請案、連續申請案、加速審查、優先權等專利申請方式,爭取及早取得專利權利及擴大保護的範圍。
因此,從雙方競爭發現,專利申請策略對專利布局的影響至為巨大,張鋒具有專利數量的優勢,但在專利的布局上以珍妮佛.道娜的專利網結構更佳,除了嫺熟專利法相關規定只是基本外,掌握申請時間及獲證時間也相對重要,並要能活用及搭配不同的策略才能達到布局中重要的防護效果。
CRISPR 技術對於未來生技產業應用的範圍甚廣,目前已進入到動物實驗階段,前景似乎看似美好,但基因訂製人所涉及的倫理與道德爭議,要如何在規範之內運作,除了技術者的能力與操守外,仍是需要社會大眾持續觀注與討論的。
參考資料
- 35 U.S.C. 111 Application, Manual of Patent Examining Procedure, USPTO, Retrieved September 5, 2017, from https://www.uspto.gov/web/offices/pac/mpep/s1417.html
- 35 U.S.C. 119 Benefit of earlier filing date; right of priority, Manual of Patent Examining Procedure, USPTO. Retrieved September 5, 2017, from https://www.uspto.gov/web/offices/pac/mpep/s601.html