文/何健民|美國維奇塔州立大學物理系榮譽講座教授
自然科學的觀念直到 19 世紀末期才進展到現代形式,它源自哲學的多向分枝中的一枝所謂自然哲學。以觀測或實驗為依據,加上基於邏輯、歸納的數學分析。15~17 世紀間,歐洲文藝復興,自然哲學成就突飛猛進,人才輩出,包括哥白尼、培根、伽利略、克卜勒和牛頓。波以耳在 17 世紀後期就提出和煉金術截然不同的觀念,但要到 19 世紀中葉,科學家才有物理、化學之分。不久又加入了生物、地質和其他學門。
到了 20 世紀,自然科學知識大幅上升,每一學門跟著逐漸細分,研究領域也變得更加寬廣。同時,跨學門、領域,甚至和技術層面的結合,形成了許多新的專長。其中一項是低溫科技,在這裡我先自問自答:
多低是低?為什麼要這麼低?
多低是低?
我的興趣是低溫物理。當被問到:你的實驗最低到幾度?我會先說明圖一中的三種溫標:攝氏(℃)或華氏(℉)為我們日常熟悉的,相對比較有科學意義的是凱爾文(Lord Kelvin,1824 – 1907)建立的凱氏(K)或絕對溫標。不同溫標間可以很方便的換算:例如水的冰點 0℃ 等於 32℉ 或 273K,而沸點 100℃ 等於 212℉ 或 373K。
攝氏、華氏都有正、負度數,但凱氏的絕對零度(0 K)是理論上低溫的極限。而我的實驗最低到 0.06K,是否就是零度?不是,離得還遠。怎麼說呢?

和我們個人生活有關的數字,一般都很簡單。例如超市內雞蛋、蘋果、牛奶的價格,或是一個學校的師生人數。 可是兩兆台幣(國家年度的總預算)就得在 2 之後加上一大堆 0。不當心少寫或多加一個 0,問題就大了。較好的方法就是用指數(exponent)改寫成 2 × 1012。同樣的,長度(L)小到奈米時,可以寫成 10−9 米。要再簡化,可以用對數觀念: Log L(米)= −9。
回到溫度:從半夜 20℃ 到正午 35℃ 間每小時的氣溫變化,用一個線性坐標圖就可顯示。但今天的科技涵蓋了非常大的溫度範圍,線性坐標不再合適,需要用對數坐標取代。
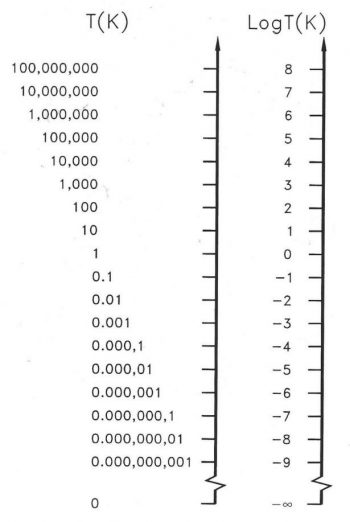
圖二中的溫區從 T = 10−9 到 108 K,或是 Log T(K) = −9 到 8。Log T(K) = 2 是常溫附近、Log T(K) = 5 以上沒有固體存在、Log T(K) = 6 已經是離子帶、而 Log T(K) = 8 接近實驗室中的最高溫。相對的,Log T(K) = −9 甚至 −10 是芬蘭的一些科學家在實驗室中達到的世界低溫紀錄。
從這圖中可以明顯看出:Log T(K) = 0 只是 T = 1 K;而可望不可及的絕對零度 T = 0 K 是在無窮遠的下方,因為 Log 0(K) = Log 10−∞ = −∞。我所達到的 0.06 K 僅在 Log T (K) = −2 和 −1 之間。可不是離絕對零度夠遙遠了嗎?
想當然的,人類對自然界的瞭解,起初都是從日常生活環境中觀察體驗的結果。冰天雪地的 −20℃ 或 −30℃ 對我們來說,已是夠冷了。但經年累月,新進技術製成了產生更低溫的設備、發明了相關的測量儀器,使得可作科學研究的最低溫度逐漸下降。
在這過程中,發現許多前所未知的自然現象,同時發展出更多有高度應用價值的工業成品。低溫科技逐漸被重視,如何達到更低溫區成了新科技的競爭目標之一。
「多低是低?」該是一個很簡單、也很實際的問題。但是它沒有絕對答案。為什麼?讓我用尺寸大小作譬喻,因為我們對大小,比對溫度有感覺得多些。俗語說「麻雀雖小,五臟俱全」。但螞蟻不是更小?單細胞生物、遺傳基因就必需用顯微鏡、甚至電子顯微鏡才看得見。往下延伸,10−10 米左右的原子中還有電子和原子核、而原子核中有更小的中子和質子。所以說,要問「多小是小?」,同樣沒有答案。
在美國加州矽谷的英特爾博物館(Intel Museum),有一個簡單的測驗,要你把一隻手掌儘快從左方移向兩呎左右間隔的右方。兩邊各有一個感應器,會測出手掌移動的時間,大概只要 0.01 秒左右,夠快了吧?但遠慢於電腦晶片工作速度,牆上標語提問:How fast is fast?「多快是快?」類似的問題可以是:「多遠是遠?」、「多貴是貴?」、甚至「多高 ( 溫 ) 是高?」。顯然,答案要看發問的討論主題是什麼。

殺雞焉用牛刀,所以需要的低溫,應該是取決於研究問題本身。從這個觀點出發,換一個問題:「為什麼要這麼低?」也許才更有意義。至於我在 0.06K 附近得到的實驗數據,是為了解瞭金屬錳的原子核中一些磁性特徵。在稍高的溫度,信號會很快減弱,同時受到晶體中的離子和電子干擾。理論上,如果能夠達到 0.01 K,甚至 0.001 K,結論會更精確,但限於技術、經費,我就只有「希望在明天」了。我會在下節文章裡,用些實例來討論。
為什麼要這麼低?
首先,借用我們的經驗:幾乎所有氣態物質(例如水蒸氣),都會隨溫度降低,發生經由液態(水),再轉成固態(冰)的相變(Phase transitions)。不過儘管今天科學已是如此發達、而這些相變又是很普通的自然現象,但任何一種物質,包括水,相變溫度仍然無法由理論計算,而必須從升溫或降溫實驗中獲得。更重要的,往低溫發展,開始可能是為了技術應用,但過程中不時會發現新的自然現象,激發科學研究,又再促成新的技術。
空氣主要成分為氧(21%)和氮(78%)。大幅降溫到 90K(−183℃),氧就會液化,氮仍是氣態。利用冷凝點的差異,可以將氧、氮分離。先收集到的液態純氧加熱氣化後,裝入高壓鋼瓶,運銷各地。它的用途很廣,包括醫療、航空、和火箭推進系統。剩下的低溫氮氣,要再低到 77K(−196℃)才液化,可以說是價廉的副產品,多用在醫學、理工研究單位、甚至食品工業。

氫是最簡單的元素,在週期表中排第一。每公升氫氣只有 0.089 克,遠低於空氣的 1.28 克,因此在空氣中,會受浮力上升。接近地層附近,沒有氫氣的自由存在。有需要時,可以從煤、天然氣 、或是石油提煉取得。當然,電解水分子(H2O)也會產生氫,只是成本太高。反向化學反應:氫在氧中燃燒,會產生相當大的能量。為太空探測,強力火箭的燃料,就是液態氧和液態氫。用液態燃料是為了火箭的體積有限。液態氫的密度比起氣態來,要高到近 800 倍,符合效率考量。但氫氣要冷到 20K(−253℃)才液化,也就有了低溫的需求。
週期表中排第二的是氦。一般人對它的認識多限於充氦的氣球,由於密度小(每公升 0.18 克),會在空氣中上升。也因為如此,接近地層附近,和氫一樣,不會有氦的自由存在。但不同於氫,因為氦是不產生任何化學反應的惰性元素,所以沒有含氦的化合物,也就無法從其他材料取得氦。幸好當地球在近 50 億年前從星際中形成時,部分原有的氦氣被陷於一些地穴中。經過長期地質、生物消長,今天已和天然氣共存。

1907 年,荷蘭萊頓大學(Leiden University)的物理學家昂內斯(Kamerlingh Onnes)首次液化從天然氣穴中分離出來的氦氣。它的冷凝點在所有氣體中最低,要到 4.2K 才由氣體變為液體。不但如此,它在常壓下、再低的溫度,也不凝固。液態氦到固態的轉變,只有在足夠的壓力下才會發生。這些現象當然都是靠低溫研究發掘出來。
回顧一段昂內斯在 1911 年的重要實驗:當時仍在現代科學起蒙階段,還沒有今天所謂的量子或是固態物理。因此實驗只是簡單的金屬電阻測量。有可能他是在尋找一種可以在低溫下適用的電阻溫度計。
溫度計的要求,是在使用的溫區中,隨著溫度變化,它有某一種性質,具有相對應的靈敏、並能重複的改變。例如日常使用的體溫計,是因為玻璃毛細管中的水銀,對溫度有較大的熱膨脹係數。當然這一類歸屬於方便、實用的溫度計,都得先對原始標準溫度計校準。後者一般是有理論基礎、但量測麻煩,不適合經常使用。

異於絕緣體的導電體,有部分電子可以在整個固體中自由運動,所以當線材兩端有電壓時產生電流。電流大小,取決於電壓和電阻。電阻的產生,是因為電子在行進中,受到導體本身離子振動影響,及雜質干擾。溫度會改變離子振幅,引發的電阻因此和溫度有關,但雜質部分不受溫度影響。在低溫時,雜質部分可以遠大於離子振動影響,使電阻失去對溫度的反應。因此,低溫下理想的電阻溫度計,勢必要是有很高純度的金屬線材。但在 20 世紀初葉,尚未有去除雜質而純化金屬的能力,當時最純的金屬就是俗稱為水銀的汞,冷凝點為 −36℃。在常溫時,仍是銀色的液體,雜質輕的上浮、重的下沈,去掉上、下層,再經蒸餾手續,就可得到純汞。
昂內斯利用液氦為冷媒,測出固態汞的電阻,它開始隨溫度下降而緩慢減低,但就在 4.2K 附近,出乎意料的現象發生了:汞的電阻突然完全消失。這種並非逐漸趨零、而是突變的現象被稱為超導轉變(Superconducting transition),和固、液、氣態間的轉變同屬自然界中的相變。
零電阻對各種電機應用設備,可以有極大貢獻。舉電磁線圈為例:即使細如髮絲的超導線,也可承載上百安培的電流,又沒有熱的產生,因此用以繞成複層線圈,維持在液氦中,通過大電流,就會產生非常高的磁場。這一類技術已普遍用在醫學檢驗中的磁共振顯像儀(Magnetic Resonance Imaging,簡稱 MRI)、和高能實驗室中的粒子加速器。
一個世紀過去了,超導轉變在許多其他元素、合金、化合物中被發現,但所有超導體的轉變溫度,都在 20K 左右以下,直到 1987 年,才有新材料被發現,轉變溫度大幅上升到 100K 附近。雖仍遠在常溫之下,但已可用量產、價廉的液氮取代液氦為冷媒。為了瞭解這些自然現象,加以由它們衍生出來的許多應用技術,「為什麼要這麼低?」又有了一些答案。
將封閉、絕熱的液氦容器減壓,抽出液面上的蒸氣,剩下的液氦溫度會隨著下降。在 2.17K,有類似超導相 (Superconductivity,電阻突然消失)的超流相(Superfluidity,黏滯性突然消失)轉變,也是自然界奇特現象。繼續減壓,一般可以達到 1K 附近。
如再細分,氦有兩種同位素(Isotopes),前面提到的液氦實際上是氦–4(He-4)。極少量的氦–3(He-3)必需從原子核反應中取得,冷凝點更低(3.2K),減壓可以達到 0.3K。利用氦–3 或氦–4 為冷媒,使得更多的研究可以在極低溫度下進行,有助我們瞭解許多材料的低溫特性。但液氦–3 是否也有超流相轉變?卻是維持了很多年,懸而未決的問題。既然在可以達到的低溫區沒有被發現,再往更低的溫度就成了工作目標。
液氦–3 和液氦–4 一樣,也只有在高壓下才會固化。但液氦–3 另有一項異於所有其他物質的特性:高壓下固化需要吸熱(其他液體固化是放熱反應),在對外絕熱情況下,熱的來源是剩餘的液體,而使後者溫度續降。當所有液氦–3 固化時,可以達到 0.002K。就是利用這種特殊的降溫技術,液氦–3 也和液氦–4 一樣,在 0.002K 顯示了超流相轉變。從 1913 年,昂內斯受頒諾貝爾物理獎以來,已有眾多科學家也獲得諾貝爾桂冠,表揚他們在研究液氦、超流相、超導及其他低溫方面的成就。
本文轉載自《物理雙月刊》38 期 8 月號,更多文章請見物理雙月刊網站。