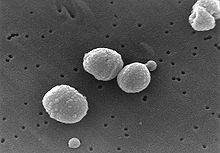
圖片來自儘管有青黴素(盤尼西林)及隨後的多種抗生素,鏈球菌屬細菌(streptococcus bacteria)一直是世界各地健康的主要威脅。原因是,該病原菌的絕佳進化能力,迅速地改變其基因組成。在一篇發表於2011年1月28日版《科學》(Science)期刊的劃時代論文中,來自美國洛克斐勒大學(Rockefeller University)及英國桑格研究所(the Sanger Institute)的科學家們業已使用全基因體排序法(full genome sequencing),來確認於肺炎鏈球菌(Streptococcus pneumoniae)之分子進化中的確切步驟。他們的研究證實,該種細菌的基因體,在及時的情況及其全球大規模的地區性散佈期間業已經歷過多次的改變。
根據世界衛生組織(the World Health Organization)的說法,據估致命的肺炎球菌病每年奪走近4百萬條人命,其中多數是未開發國家的孩童。人類不但是肺炎球菌病的原始對象,而且是主要代表。因而,於咱們地球上,人類很可能是該移生於學齡前兒童鼻咽中之菌種僅有的生態儲藏所(ecological reservoir)。
這些由英國桑格研究所Stephen D. Bentley領導的研究人員,將高解析的基因體排序法使用於,由包括洛克斐勒大學Alexander Tomasz領導的微生物學暨傳染病實驗室等諸多合作實驗室提供之肺炎鏈球菌的臨床分離物(clinical isolates)上。藉由有關此些分離物之年代、地理位置及感染部位等可資取得的數據,Bentley及同僚們能出示有關一種具抗多種藥物性,被通稱為PMEN無性繁殖系1(the PMEN clone 1)之肺炎鏈球菌的無性繁殖系個體進化路徑圖。
此些科學家確認,該極度發跡之抗多種藥物的無性繁殖系,其可能的起源年代及地點是在1970年及歐洲。之後該無性繁殖系散播到南、北美洲、南非及亞洲。於2001年,Tomasz的團隊證實,該無性繁殖系存在於美國紐約市12家醫院。或許更重要的是,此些研究發現提供了,於肺炎鏈球菌中,遺傳改變的機制主要是透過基因重新組合,不是獲得點突變(point mutations)的證據。
Tomasz宣稱:「導致Oswald Avery及其洛克斐勒大學的同僚們,於1944年確認DNA為遺傳物質的遺傳轉化(genetic transformation)現象,是肺炎鏈球菌在其真正生物體內之環境中,進化期間使用的特殊方法。」
於實驗室中,首度被確認的其他現象,也出現於肺炎鏈球菌在生物體內進化的諸階段中。譬如,在臨床分離物中被觀察到的諸多重新組合,至少有些改變似乎使用了”感受性”系統(competence system)。這是由一種於實驗室中,首度被Tomasz及同僚們發現之特有細菌群體感知作用物(bacterial quorum sensing agent)所誘發的DNA吸收機制。同樣地,抗青黴素的機制經證實涉及從其他細菌引入基因。這是先前於個體抗青黴素分離物之諸多研究中,經文獻佐證的發現。該機制於1980年代,首度被Tomasz及同僚們確認,是青黴素標的蛋白質之親和力中的諸多改變。此些蛋白質也被通稱為青黴素結合蛋白質(penicillin binding proteins:PBPs)。
Tomasz宣稱:「或許,該項研究最吸引人的部分是記述了,在諸如引進青黴素、其他抗生素及最近引進共軛抗肺炎鏈球菌疫苗(conjugate anti-pneumococcal vaccines)的臨床環境中,該無性繁殖系已如何迅速地對生物體內的大量介入物作出反應。上述疫苗是針對最多血清型的該種細菌,此些細菌於孩童的鼻咽中傳播且引發侵犯性疾病。」
Tomasz宣稱:「該項研究也證實了,像在高解析之基因體分析上具有專長的桑格研究所及咱們能夠提供徹底表現出特徵之細菌分離物的實驗室等團隊間密切合作的重要性。這類型的合作十分符合洛克斐勒大學,從事諸多結合臨床與轉譯科學(translational science)之研究的傳統。此類分子生物學與流行病學間的結合,可望進一步地有助於洞察細菌於生物體內的進化機制。這最終可能使人們得以瞭解,儘管其他細菌相繼死亡,為何PMEN-1該無性繁殖系能如此廣泛散播的秘密。
原文網址:http://newswire.rockefeller.edu/?page=engine&id=1139
翻譯:peregrine