本文與 TRPMA 台灣研發型生技新藥發展協會合作,泛科學企劃執行
我們知道癌症是台灣人健康的頭號公敵。 為此,我們花了很多時間介紹最新、最有效的抗癌方法之一:免疫療法 。
免疫療法中最重要的技術就是抗體藥物。科學家會人工製造一批抗體去標記癌細胞。它們就像戰場上的偵察無人機,能精準鎖定你體內的敵人——癌細胞,為它們打上標記,然後引導你的免疫系統展開攻擊。
這跟化療、放射線治療那種閉著眼睛拿機槍亂掃不同。免疫療法是重新叫醒你的免疫系統,為身體「上buff (增益) 」來抗癌,副作用較低,因此備受好評。
但尷尬的是 ,經過幾年的臨床考驗,科學家發現:光靠抗體對抗癌症,竟然已經不夠用了。
事情是這樣的,臨床上醫生與科學家逐漸發現:這個抗體標記,不是容易損壞,就是癌細胞同時設有多個陷阱關卡,只靠叫醒免疫細胞,還是難以發揮戰力。
但好消息是,我們的生技工程也大幅進步了。科學家開始思考:如果這台偵察無人機只有「標記」這一招不夠用,為什麼不幫它升級,讓它多學幾招呢?
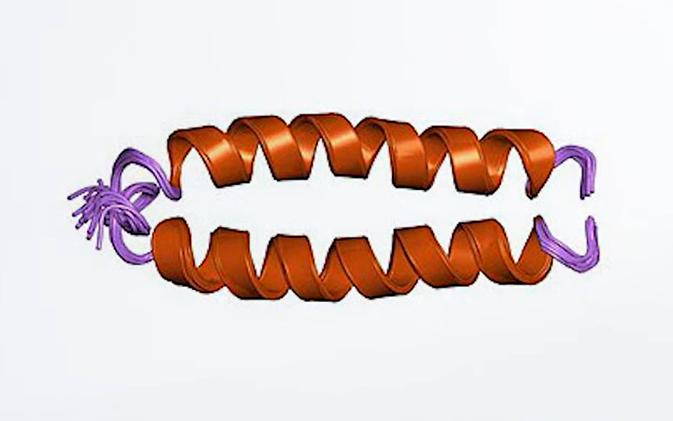
這個能讓免疫藥物(偵察無人機)大進化的訓練器,就是今天的主角—融合蛋白(fusion protein) 。
融合蛋白(fusion protein) / 圖片來源:wikipedia
融合蛋白是什麼? 免疫療法遇到的問題,我們可以這樣理解:想像你的身體是一座國家,病毒、細菌、腫瘤就是入侵者;而抗體,就是我們派出的「偵察無人機」。
當我們透過注射放出這支無人機群進到體內,它能迅速辨識敵人、緊抓不放,並呼叫其他免疫單位(友軍)一同解決威脅。過去 20 年,最強的偵查機型叫做「單株抗體」。1998年,生技公司基因泰克(Genentech)推出的藥物赫賽汀(Herceptin),就是一款針對 HER2 蛋白的單株抗體,目標是治療乳癌。
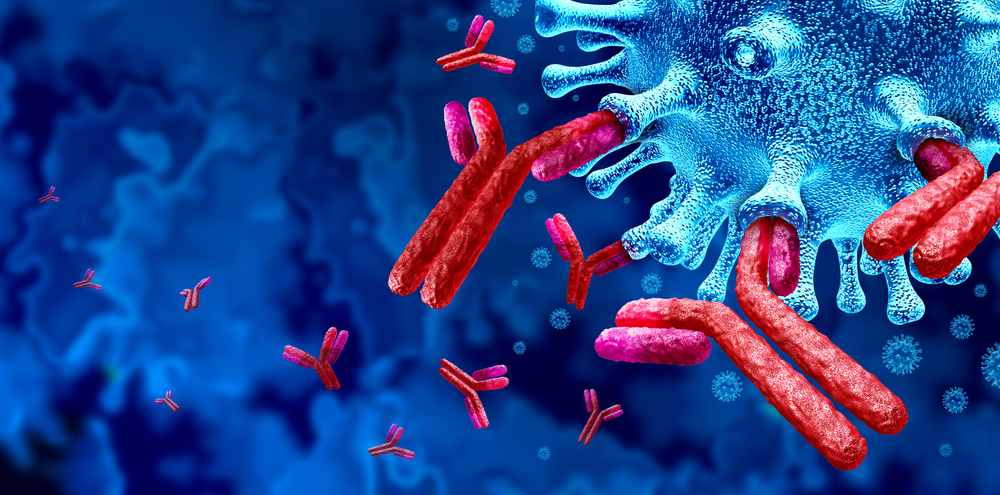
這支無人機群為什麼能對抗癌症?這要歸功於它「Y」字形的小小抗體分子,構造看似簡單,卻蘊藏巧思:
「Y」 字形上面的兩隻「叉叉」是敵人偵測器,能找到敵人身上的抗原特徵,並黏上去,稱為抗體結合區「Fab 區域」。
「Y」 字形的「尾巴」就是我們說的「標籤」,它能通知免疫系統啟動攻擊,稱為結晶區域片段「Fc 區域」。具體來說,當免疫細胞在體內巡邏,免疫細胞上的 Fc 受體 (FcR) 會和 Fc區域結合,進而認出病原體或感染細胞,接著展開清除。
更厲害的是,這個 Fc 區域標籤還能加裝不同功能。一般來說,人體內多餘的分子,會被定期清除。例如,細胞內會有溶酶體不斷分解多餘的物質,或是血液經過肝臟時會被代謝、分解。那麼,人造抗體對身體來說,屬於外來的東西,自然也會被清除。
而 Fc區域會與細胞內體上的Fc受體結合,告訴細胞「別分解我」的訊號,阻止溶酶體的作用。又或是單純把標籤做的超大,例如接上一段長長的蛋白質,或是聚乙二醇鏈,讓整個抗體分子的大小,大於腎臟過濾孔的大小,難以被腎臟過濾,進而延長抗體在體內的存活時間。
偵測器(Fab)加上標籤(Fc)的結構,使抗體成為最早、也最成功的「天然設計藥物」。然而,當抗體在臨床上逐漸普及,一個又一個的問題開始浮現。 抗體的強項在於「精準鎖定」,但這同時也是它的限制。
「Y」 字形上面的兩隻「叉叉」是敵人偵測器,能找到敵人身上的抗原特徵,並黏上去,稱為抗體結合區「Fab 區域」/ 圖片來源:shutterstock
第一個問題:抗體只能打「魔王」,無法毀掉「魔窟」。
抗體一定要有一個明確的「標的物」才能發揮作用。這讓它在針對「腫瘤」或「癌細胞本身」時非常有效,因為敵人身上有明顯標記。但癌細胞的形成與惡化,是細胞在「生長、分裂、死亡、免疫逃脫」這些訊號通路上被長期誤導的結果。抗體雖然勇猛,卻只能針對已經帶有特定分子的癌細胞魔王,無法摧毀那個孕育魔王的系統魔窟。這時,我們真正欠缺的是能「調整」、「模擬」或「干擾」這些錯誤訊號的藥物。
第二個問題:開發產線的限制。
抗體的開發,得經過複雜的細胞培養與純化程序。每次改變結構或目標,幾乎都要重新開發整個系統。這就像你無法要求一台偵測紅外線的無人機,明天立刻改去偵測核輻射。高昂的成本與漫長的開發時間,讓新產線難以靈活創新。
為了讓免疫藥物能走向多功能與容易快速製造、測試的道路,科學家急需一個更工業化的藥物設計方式。雖然我們追求的是工業化的設計,巧合的是,真正的突破靈感,仍然來自大自然。
在自然界中,基因有時會彼此「融合」成全新的組合,讓生物獲得額外功能。例如細菌,它們常仰賴一連串的酶來完成代謝,中間產物要在細胞裡來回傳遞。但後來,其中幾個酶的基因彼此融合,而且不只是基因層級的合併,產出的酶本身也變成同一條長長的蛋白質。
結果,反應效率大幅提升。因為中間產物不必再「跑出去找下一個酶」,而是直接在同一條生產線 上完成。對細菌來說,能更快處理養分、用更少能量維持生存,自然形成適應上的優勢,這樣的融合基因也就被演化保留下來。
科學家從中得到關鍵啟發:如果我們也能把兩種有用的蛋白質,「人工融合」在一起,是否就能創造出更強大的新分子?於是,融合蛋白(fusion protein)就出現了。
以假亂真:融合蛋白的HIV反制戰 融合蛋白的概念其實很直覺:把兩種以上、功能不同的蛋白質,用基因工程的方式「接起來」,讓它們成為同一個分子。
1990 年,融合蛋白 CD4 免疫黏附素(CD4 immunoadhesin)誕生。這項設計,是為了對付令人類聞風喪膽的 HIV 病毒。
我們知道 T 細胞是人體中一種非常重要的白血球。在這些 T 細胞中,大約有六到七成表面帶有一個叫做「CD4」的輔助受體。CD4 會和另一個受體 TCR 一起合作,幫助 T 細胞辨識其他細胞表面的抗原片段,等於是 T 細胞用來辨認壞人的「探測器」。表面擁有 CD4 受體的淋巴球,就稱為 CD4 淋巴球。
麻煩的來了。 HIV 病毒反將一軍,竟然把 T 細胞的 CD4 探測器,當成了自己辨識獵物的「標記」。沒錯,對 HIV 病毒來說,免疫細胞就是它的獵物。HIV 的表面有一種叫做 gp120 的蛋白,會主動去抓住 T 細胞上的 CD4 受體。
一旦成功結合,就會啟動一連串反應,讓病毒外殼與細胞膜融合。HIV 進入細胞內後會不斷複製並破壞免疫細胞,導致免疫系統逐漸崩潰。
為了逆轉這場悲劇,融合蛋白 CD4 免疫黏附素登場了。它的結構跟抗體類似,由由兩個不同段落所組成:一端是 CD4 假受體 ,另一端則是剛才提到、抗體上常見的 Fc 區域 。當 CD4 免疫黏附素進入體內,它表面的 CD4 假受體會主動和 HIV 的 gp120 結合。
厲害了吧。 病毒以為自己抓到了目標細胞,其實只是被騙去抓了一個假的 CD4。這樣 gp120 抓不到 CD4 淋巴球上的真 CD4,自然就無法傷害身體。
而另一端的 Fc 區域則有兩個重要作用:一是延長融合蛋白在體內的存活時間;二是理論上 能掛上「這裡有敵人!」的標籤,這種機制稱為抗體依賴性細胞毒殺(ADCC)或免疫吞噬作用(ADCP)。當免疫細胞的 Fc 受體與 Fc 區域結合,就能促使免疫細胞清除被黏住的病毒顆粒。
不過,這裡有個關鍵細節。
在實際設計中,CD4免疫黏附素的 Fc 片段通常會關閉「吸引免疫細胞」的這個技能。原因是:HIV 專門攻擊的就是免疫細胞本身,許多病毒甚至已經藏在 CD4 細胞裡。若 Fc 區域過於活躍,反而可能引發強烈的發炎反應,甚至讓免疫系統錯把帶有病毒碎片的健康細胞也一併攻擊,這樣副作用太大。因此,CD4 免疫黏附素的 Fc 區域會加入特定突變,讓它只保留延長藥物壽命的功能,而不會與淋巴球的 Fc 受體結合 ,以避免誘發免疫反應。
從 DNA 藍圖到生物積木:融合蛋白的設計巧思 融合蛋白雖然潛力強大,但要製造出來可一點都不簡單。它並不是用膠水把兩段蛋白質黏在一起就好。「融合」這件事,得從最根本的設計圖,也就是 DNA 序列就開始規劃。
我們體內的大部分蛋白質,都是細胞照著 DNA 上的指令一步步合成的。所以,如果科學家想把蛋白 A 和蛋白 B 接在一起,就得先把這兩段基因找出來,然後再「拼」成一段新的 DNA。
不過,如果你只是單純把兩段基因硬接起來,那失敗就是必然的。因為兩個蛋白會互相「打架」,導致摺疊錯亂、功能全毀。
這時就需要一個小幫手:連接子(linker) 。它的作用就像中間的彈性膠帶,讓兩邊的蛋白質能自由轉動、互不干擾。最常見的設計,是用多個甘胺酸(G)和絲胺酸(S)組成的柔性小蛋白鏈。
設計好這段 DNA 之後,就能把它放進細胞裡,讓細胞幫忙「代工」製造出這個融合蛋白。接著,科學家會用層析、電泳等方法把它純化出來,再一一檢查它有沒有摺疊正確、功能是否完整。
如果一切順利,這個人工設計的融合分子,就能像自然界的蛋白一樣穩定運作,一個全新的「人造分子兵器」就此誕生。
CD4免疫黏附素問世之後,融合蛋白逐漸成為生物製藥的重要平台之一。而且現在的融合蛋白,早就不只是「假受體+Fc 區域」這麼單純。它已經跳脫模仿抗體,成為真正能自由組裝、自由設計的生物積木。
CD4免疫黏附素問世之後,融合蛋白逐漸成為生物製藥的重要平台之一 / 圖片來源:wikipedia
融合蛋白的強項,就在於它能「自由組裝」。
以抗體為骨架,科學家可以接上任何想要的功能模組,創造出全新的藥物型態。一般的抗體只能「抓」(標記特定靶點);但融合蛋白不只會抓,還能「阻斷」、「傳遞」、甚至「調控」訊號。在功能模組的加持下,它在藥物設計上,幾乎像是一個分子級的鋼鐵蜘蛛人裝甲。
一般來說,當我們選擇使用融合蛋白時,通常會期待它能發揮幾種關鍵效果:
療效協同: 一款藥上面就能同時針對多個靶點作用,有機會提升治療反應率與持續時間,達到「一藥多效」的臨床價值。減少用藥: 原本需要兩到三種單株抗體聯合使用的療法,也許只要一種融合蛋白就能搞定。這不僅能減少給藥次數,對病人來說,也有機會因為用藥減少而降低治療成本。降低毒性風險: 經過良好設計的融合蛋白,可以做到更精準的「局部活化」,讓藥物只在目標區域發揮作用,減少副作用。
到目前為止,我們了解了融合蛋白是如何製造的,也知道它的潛力有多大。
那麼,目前實際成效到底如何呢?
一箭雙鵰:拆解癌細胞的「偽裝」與「內奸」 2016 年,德國默克(Merck KGaA)展開了一項全新的臨床試驗。 主角是一款突破性的雙功能融合蛋白──Bintrafusp Alfa。這款藥物的厲害之處在於,它能同時封鎖 PD-L1 和 TGF-β 兩條免疫抑制路徑。等於一邊拆掉癌細胞的偽裝,一邊解除它的防護罩。
PD-L1,我們或許不陌生,它就像是癌細胞身上的「偽裝良民證」。當 PD-L1 和免疫細胞上的 PD-1 受體結合時,就會讓免疫系統誤以為「這細胞是自己人」,於是放過它。我們的策略,就是用一個抗體或抗體樣蛋白黏上去,把這張「偽裝良民證」封住,讓免疫系統能重新啟動。
但光拆掉偽裝還不夠,因為癌細胞還有另一位強大的盟友—一個起初是我軍,後來卻被癌細胞收買、滲透的「內奸」。它就是,轉化生長因子-β,縮寫 TGF-β。
先說清楚,TGF-β 原本是體內的秩序管理者,掌管著細胞的生長、分化、凋亡,還負責調節免疫反應。在正常細胞或癌症早期,它會和細胞表面的 TGFBR2 受體結合,啟動一連串訊號,抑制 細胞分裂、減緩 腫瘤生長。
但當癌症發展到後期,TGF-β 跟 TGFBR2 受體之間的合作開始出問題。癌細胞表面的 TGFBR2 受體可能突變或消失,導致 TGF-β 不但失去了原本的抑制作用,反而轉向幫癌細胞做事 。
它會讓細胞骨架(actin cytoskeleton)重新排列,讓細胞變長、變軟、更有彈性,還能長出像觸手的「偽足」(lamellipodia、filopodia),一步步往外移動、鑽進組織,甚至進入血管、展開全身轉移。
更糟的是,這時「黑化」的 TGF-β 還會壓抑免疫系統,讓 T 細胞和自然殺手細胞變得不再有攻擊力,同時刺激新血管生成,幫腫瘤打通營養補給線。
為了對抗這個內奸,默克在 Bintrafusp Alfa 的結構裡,加上了一個「TGF-β 陷阱(trap) 」。就像 1989 年的 CD4 免疫黏附素用「假受體」去騙 HIV 一樣,這個融合蛋白在體內循環時,會用它身上的「陷阱」去捕捉並中和游離的 TGF-β。這讓 TGF-β 無法再跟腫瘤細胞或免疫細胞表面的天然受體結合,從而鬆開了那副壓抑免疫系統的腳鐐。
為了對抗這個內奸,默克在 Bintrafusp Alfa 的結構裡,加上了一個「TGF-β 陷阱(trap) 」/ 情境圖來源:shutterstock
告別單一解方:融合蛋白的「全方位圍剿」戰 但,故事還沒完。我們之前提過,癌細胞之所以難纏,在於它會發展出各種「免疫逃脫」策略。
而近年我們發現,癌細胞的「偽良民證」至少就有兩張:一張是 PD-L1 ;另一張是 CD-47 。CD47 是癌細胞向巨噬細胞展示的「別吃我」訊號,當它與免疫細胞上的 SIRPα 結合時,就會抑制吞噬反應。
為此,總部位於台北的漢康生技,決定打造能同時對付 PD-L1、CD-47,乃至 TGF-β 的三功能生物藥 HCB301。
雖然三功能融合蛋白聽起來只是「再接一段蛋白」而已,但實際上極不簡單。截至目前,全球都還沒有任何三功能抗體或融合蛋白批准上市,在臨床階段的生物候選藥,也只佔了整個生物藥市場的 1.6%。
漢康生技透過自己開發的 FBDB 平台技術 ,製作出了三功能的生物藥 HCB301,目前第一期臨床試驗已經在美國、中國批准執行。
免疫療法絕對是幫我們突破癌症的關鍵。但我們也知道癌症非常頑強,還有好幾道關卡我們無法攻克。既然單株抗體在戰場上顯得單薄,我們就透過融合蛋白,創造出擁有多種功能模組的「升級版無人機」。
融合蛋白強的不是個別的偵查或阻敵能力,而是一組可以「客製化組裝 」的平台,用以應付癌細胞所有的逃脫策略。
Catch Me If You Can?融合蛋白的回答是:「We Can.」
未來癌症的治療戰場,也將從尋找「唯一解」,轉變成如何「全方位圍剿」癌細胞 ,避免任何的逃脫。