本文轉載自中央研究院「研之有物」,為「中研院廣告」
- 採訪撰文/歐宇甜
- 責任編輯/簡克志
- 美術設計/蔡宛潔
認識神經科學家程淮榮
中央研究院「研之有物」專訪院內分子生物研究所所長程淮榮特聘研究員,他認為從事基礎研究,興趣相當重要,他對神經科學的熱愛程度是每天 24 小時!最初他是熱愛解剖學的醫科生,赴哈佛深造期間,他投入了神經拓撲學領域,探索神經元如何連到正確的對應位置。回臺灣中研院之後,繼續研究與大腦記憶相關的「海馬體」。程淮榮團隊近年發現,老鼠年長之後,雖有新生的神經元,但必須排除其他舊軸突方能形成新突觸,原本存在的記憶會被清除與消失。未來,程淮榮將繼續解開成體新生神經元與海馬體的謎團!

「研之有物」先前已經報導過程淮榮長期研究的軸突導向(Axon guidance)議題,詳細讀者可以參考這篇〈當神經元遇見真愛!突觸形成的奇妙旅程〉,本文要更進一步談談關於程淮榮個人經歷,以及他最近的研究主題。
(編按:以下以問答形式呈現專訪內容,內文皆為受訪者的第一人稱視角)
一開始先請老師談談您的求學歷程吧~
我在雲林縣虎尾鎮出生,高中前往臺北念師大附中的科學實驗班,後來考上臺灣大學醫學系,至今仍然深深覺得一個二十出頭的小伙子能學習有關人類身體的龐大知識,真是一件相當神奇的事。那時我很喜歡大體解剖的課,大三有一天在臺北忠孝東路等公車,摸著手腕上剛剛學到的九條肌腱, 默念著他們如何拉著手上不同的手指頭, 抬頭看到到站公車車門轉動,突然意識到:「唉呀,這跟手掌的肌腱在牽引肌肉活動好像喔,我們的身體不就像是機械裝置嗎?這個領悟對我的影響很大。」
學習醫學讓我有機會徹底了解自己身體的各種生理構造和功能,以及疾病的成因,收穫很大。身邊的朋友或親戚有什麼疾病往往都會來問我。其實,我和中研院之間的緣分在升大五時就結下了,那時我跟同學一起去找錢煦院士,進入生醫所籌備處當暑期實習生,發現做實驗很有趣。大七開始實習後,原本我的目標是去當外科醫生。當外科醫生需要一點天份、手也要巧,我自認手蠻巧,應該很適合。
既然您很喜歡醫學,也想當外科醫生,為何之後會改變志向呢?
當外科醫師其實蠻有成就感,只要刀開一開,可能不久之後,病患就可以活蹦亂跳。我曾去過顯微骨科醫師的實驗室學習顯微手術實驗,所謂骨科的顯微手術可能就是將腳趾頭接到意外斷掉的手指上,所以我覺得很有趣、很想去學。當時老師還囑咐我,做顯微手術之前不能喝咖啡或茶,我不信邪,想說自己的手很穩,不會有問題吧。沒想到在接兔子耳朵的血管時,在顯微鏡下看到兩隻手都一直不停抖動,從此乖乖遵命。
當外科醫生只需要知道怎麼做手術就好,不過,我很希望知道更多,尤其想了解各種疾病的致病機轉, 心想也許人生還能做一點其他的事,於是決定出國去看看。我很感謝父母都支持我自由的發展,沒有勉強我要留下來開業賺錢。
出國深造期間,您在哈佛大學時曾獲得分子生物學大獎,是什麼研究呢?
哈哈,當初申請哈佛大學時,其實我的讀書計畫是想要以學習發育生物學來發展癌症治療的方法,但後來得獎的題目是神經拓撲學(Neuronal topographic mapping),探討神經元如何依照相對位置連接成一個系統。
這門學問歷史非常悠久, 最早是由 17 世紀初的哲學家和科學家笛卡兒(René Descartes)所提出。近代比較相關的一個例子, 是在 20 世紀初,有位神經外科醫生叫做懷爾德·潘菲爾德(Wilder Penfield),經過對於病人的仔細研究,他發現身體的感覺系統和運動系統可以在腦部的對應區域畫出來。而且神經越密集、越敏感的部位如手和嘴唇,在腦部占的區域越大。此外,身體各部位的神經連到腦部相對關係必須維持一樣,一點對一點,也就是所謂的拓撲圖(Topographic map),這樣我們才能正確感知外界訊息並且做出正確的運動反應。
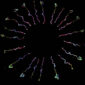
但是,神經連結不是一次到位,一個神經元要經過多次轉接到另一個神經元,最後才連到腦部正確位置。例如外界訊息進入眼睛,透過視神經連到腦部,眼睛接收到右邊視野的訊號必須達到大腦左邊的視覺區。 因此了解這些神經元在發育過程中如何連結,如何維持彼此的相對位置,就是神經拓撲學所要研究的範圍。了解神經元連結的過程很重要,例如:眼科醫師能運用視覺和腦部視覺區的拓撲圖,測試病人兩眼的視野是否正常,判斷可能是哪段神經出問題。
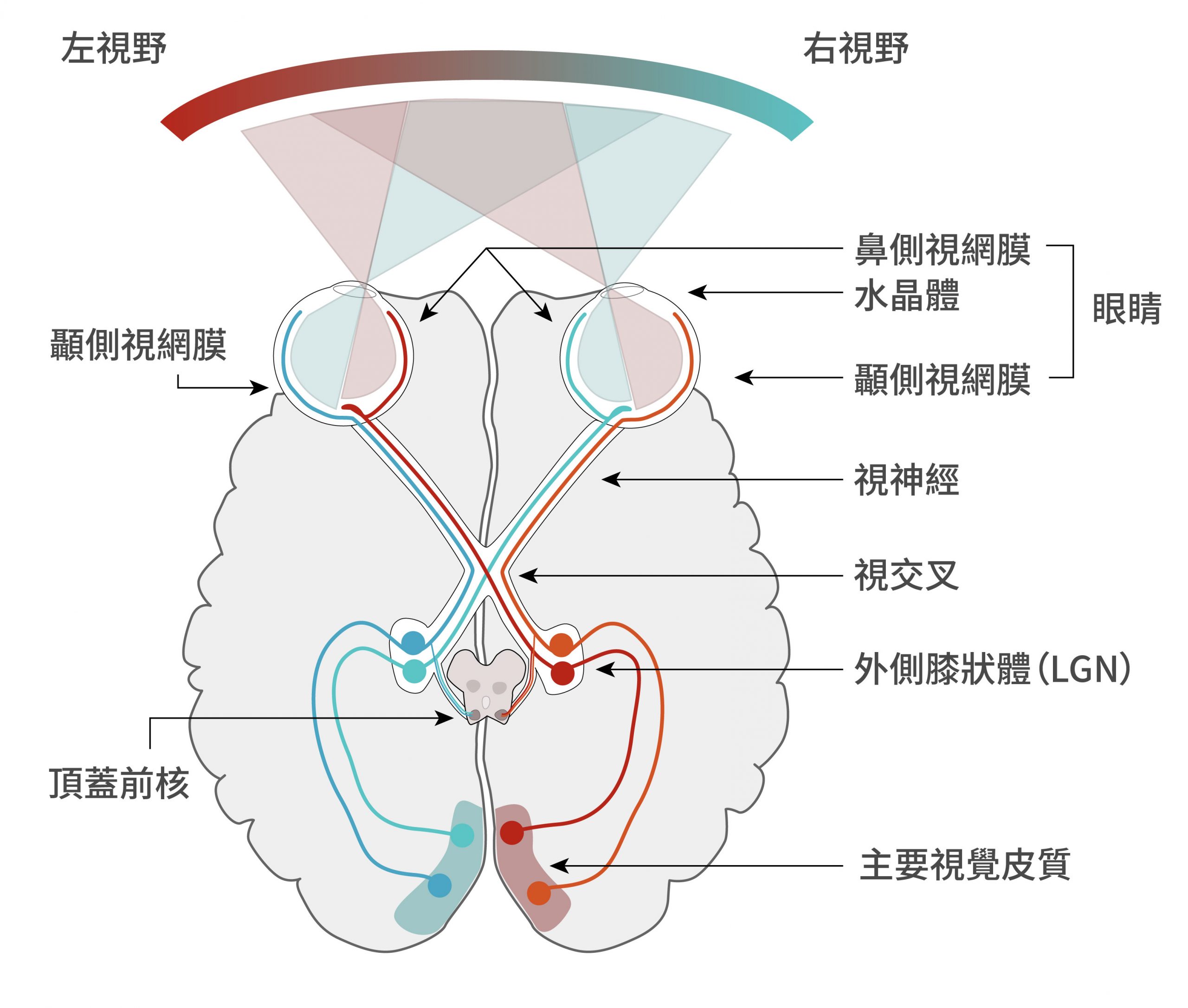
如何證明這些神經元在形成拓撲圖的過程當中可以自己找到正確的連結呢?有位美國科學家羅傑・斯佩里(Roger W. Sperry)曾經做了一個非常有名的實驗,他將青蛙眼球取出、切斷視神經,再將眼球在眼眶中旋轉 180 度後放回去。不久後青蛙眼球會再生新的視神經連到腦部,但是由於眼球內的視神經元旋轉了 180 度,但是大腦內的神經元並沒有跟著旋轉,所以這一隻青蛙從此看到的世界是上下左右顛倒:昆蟲在右上方,牠卻朝左下方伸出舌頭!
的確很神奇!神經元數量這麼多,居然都能連到正確位置。
沒錯,所以很多科學家都想知道,神經系統的拓撲圖是怎麼正確連接的?假設我們請 100 個人排隊,每個人都有意識,聽到指令會依序排好。但神經元沒有意識,如果要靠不同基因下指令連接,人體基因才幾萬個,沒辦法負荷。因此,科學家推測神經元的拓撲圖連結是靠少數分子在不同的神經元上形成不同的濃度來調控, 也就是所謂的分子梯度(Molecular gradient),這樣只需少數幾個基因即可。
例如,從眼睛到腦部有成千上萬個神經元需要連接,如果有一種分子在每個生長錐上的濃度不同,從 1、2、3 到 100,與之對應的樹突上的分子濃度也是 1 到 100,假設連接指令是將雙方濃度加起來等於 101,就可以讓生長錐的 100 接到樹突的 1,接下來 99 接到 2,98 接到 3……以此類推,就能讓神經元按正確的對應位置連接。我在哈佛時就是找出這個關鍵分子而獲得北美 Pharmacia 生物技術與科學獎(Pharmacia Biotech & Science Prize for Young Scientists in Molecular Biology)。
您離開哈佛後,接下來仍持續投入神經科學研究嗎?
是的。我先是到美國加州大學舊金山分校和史丹佛大學做博士後研究,接著到美國加州大學戴維斯分校待很長一段時間,做過許多神經科學相關的研究,像神經軸突連結如何形成(Axon guidance)、神經系統的剪枝(Pruning)等。上課時為了讓學生對神經科學產生興趣,常絞盡腦汁思考如何用比喻或故事說明。
近年回到臺灣後,接任中研院分生所的所長,雖然常要處理繁瑣的行政事務,但對我來說,這是不一樣的人生挑戰,也覺得很幸運。因為中研院分子生物研究所是全臺灣最好的,可以跟一群優秀的科學家一同研究討論,是非常難得的經驗!我也重新建立起自己的實驗室,延續在加州大學戴維斯分校進行的海馬體研究。
什麼是海馬體(Hippocampus)呢?它的功能是什麼?
我來介紹一下。神經科學史上曾有一個著名病人叫做亨利・莫雷森(Henry Molaison,生前為了保護隱私稱為 H.M.)。由於他年輕時會發作嚴重的癲癇,醫師認為可能是海馬體異常放電而引起,因此將他兩側的海馬體都切除,結果發現他的記憶從此受到影響。他記得小時候住在舊金山的街道名稱,卻不記得昨天發生的事,此時科學家才知道原來海馬體對學習與記憶有重要影響,負責將短期記憶轉譯為長期記憶。
神經系統最重要的功能之一就是記憶,神經連結需要持續存在到生物體死亡,我們才會記得過去發生的事情並避免再次犯錯。如果所有的神經細胞不斷更新,神經連結也消失,那麼記憶會完全消失,我們就無法回憶過去的經驗。
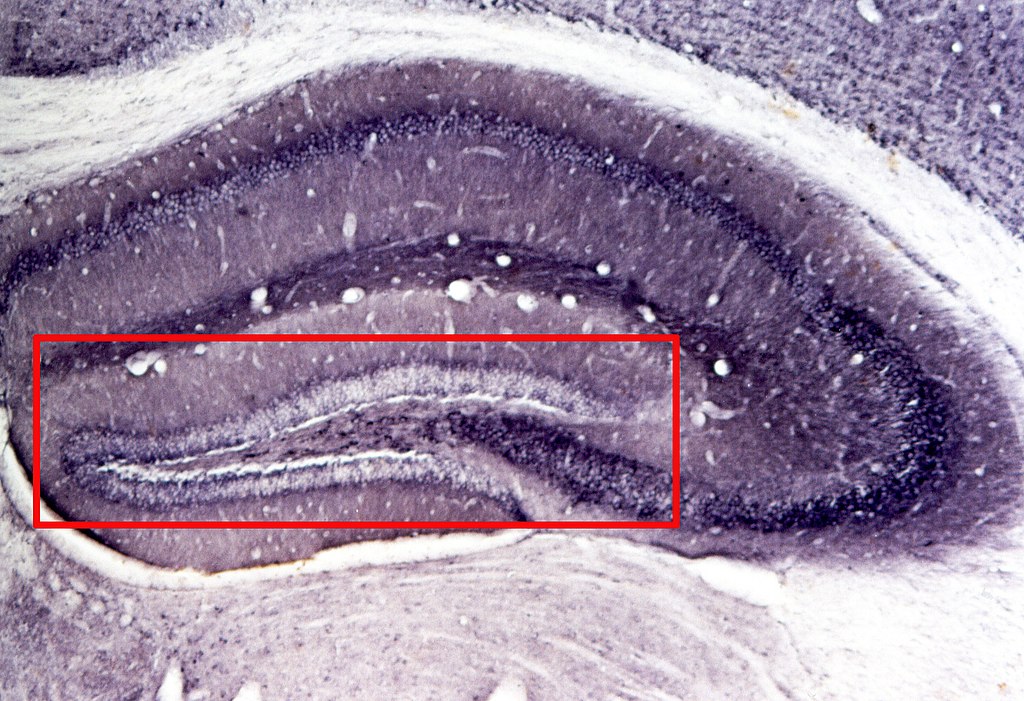
不過,現在研究已發現,成年老鼠的海馬體有個區域稱為齒狀回(Dentate gyrus),仍然會長出新的神經元,這現象稱為成體神經新生(Adult neurogenesis)。至於人類海馬體是否也具有神經元不斷新生的能力,目前科學家的觀點尚未達成一致,仍需進一步研究。
您是研究海馬體的哪個方面呢?
我很好奇的是,實驗鼠的海馬體除了新生神經元區域之外,其他部位的神經元都是存在很久的神經網路,運作也正常。這些新生神經元是如何整合進入一個成熟的神經網路,且不會影響到原有運作呢?這就好比一群孩子要進入大人的群體與他們牽手,最後融入他們的社會。
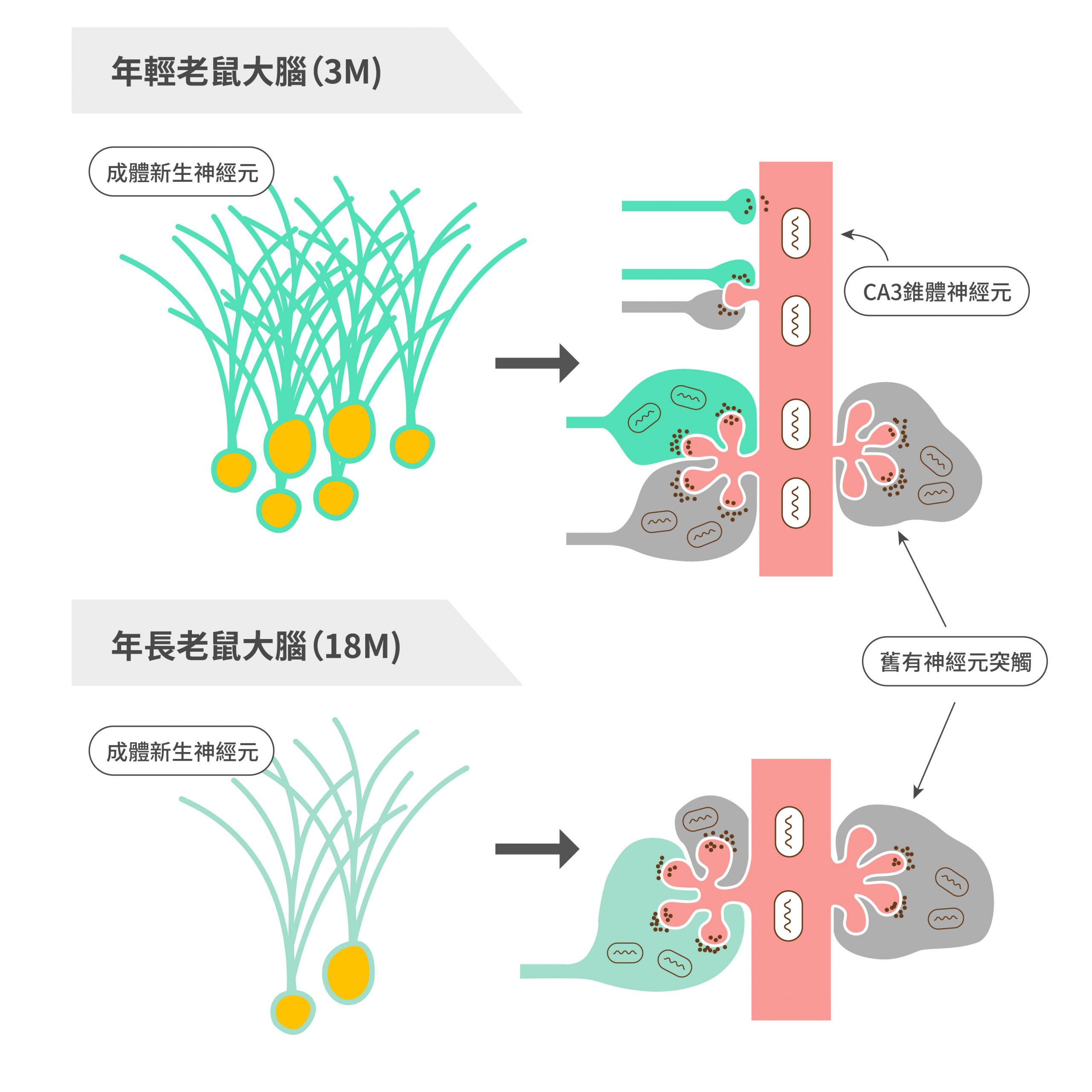
我們發現到一些有趣機制:如果是 3 個月大的老鼠(相當於人類 20 歲左右),這時原本神經元長出樹突棘的能力高,新生神經元可以直接與之形成突觸;或是趕走其他佔位置的舊軸突,以形成新突觸。但如果是 18 個月大的老鼠(相當於人類 70 歲左右),長出樹突棘的能力下降,新生神經元就只能踢開其他軸突,才能形成新突觸。
這代表,年紀大時,新生神經元唯有踢走其他軸突才能形成新突觸,原本存在的記憶會被清除與消失。年紀小時,新生神經元即使不用踢走其他軸突,仍有機會形成新突觸,記憶力比較強。
此外,我們團隊觀察到,年輕老鼠的新生神經元到完全整合進入成熟的神經網路需要 8 週時間。不過,如果齒狀回一直持續新生神經元,海馬體是否會隨年紀而變越來越大?或者有些神經元會凋亡?這是我接下來很想要破解的謎團。
神經科學研究時通常都用老鼠做實驗嗎?
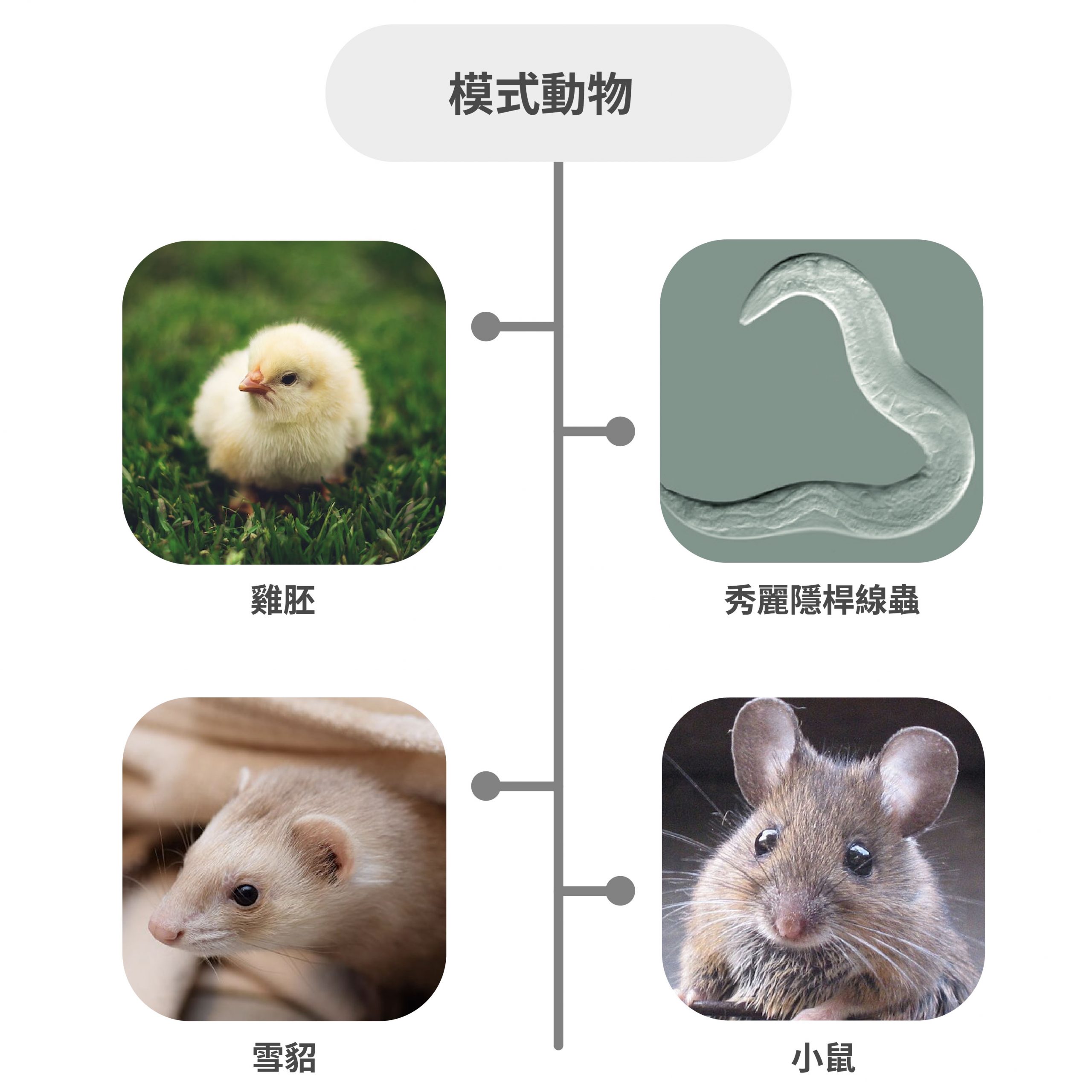
為了解釋特定生命現象或機制,由科學家廣泛採用且研究詳盡的生物,稱為模式動物。我過去曾經使用過的模式動物有線蟲、雞胚、老鼠和雪貂等。線蟲的神經數量少,每根神經、每個軸突都能看得很清楚。雪貂的體型較大,常用來作視覺和電生理研究。雞胚可以透過控制環境溫度,讓胚胎生長或停滯。老鼠的基因則跟人比較相近,但養起來很花時間。
各種模式動物有不同特性,適合不同的研究目的,目前我有許多研究都用老鼠來做。雖然了解人類神經系統是最重要的事,但科學家很難直接用人類做實驗,因此這些模式動物對人類的貢獻非常大,相當重要。

我認為,基礎科學研究是一種等待意外發現的過程,這點跟應用科學研究不大一樣。我常鼓勵學生做實驗不要怕重複,要持續不斷去做。我以前喜歡做解剖,相同實驗會一直重複做,因為不斷重複去做才可能有意外發現。
例如某次實驗原本以為結果會跟之前一模一樣,卻突然發現有某處不一樣!我喜歡稱之為 Eureka Moment(恍然大悟的時刻),據說是阿基米德在浴缸洗澡時領悟分辨王冠真偽方法而大喊「Eureka!」。另一個相關名詞是 Serendipity,是指「意外發現」,代表沒辦法計畫的偶發事件,我也很喜歡。
基礎研究最棒的獎勵大概就是這意外發現的時刻,雖然我不過碰上兩、三次大的意外發現而已,但每次碰到就覺得無比開心!只是這感覺有時很難說明,要自己親身體驗才知道。
另外,我認為興趣很重要,並不是每個人都適合做基礎研究、當科學家。人人都是獨立個體,腦袋都不一樣,尤其這世界變化得很快、很難預測未來,因此,最重要的是去發掘自己的能力,找出擅長做的事。那什麼才是喜歡做的事呢?就是幾乎 24 小時都會想到它,甚至連睡覺都夢到,不會說下班五點後就不想它。如果人生可以一直做自己喜歡的事,那就是最幸運的事了!

延伸閱讀
- 程淮榮個人頁面
- 歐宇甜(2023)。〈當神經元遇見真愛!突觸形成的奇妙旅程〉,《研之有物》。
- 中研講堂離島首場 400 位金門師生 一窺量子與神經科學的奧秘 | 中研院訊 (sinica.edu.tw)
- Murray, K. D., Liu, X.-B., King, A. N., Luu, J. D., & Cheng, H.-J. (2020). Age-related changes in synaptic plasticity associated with mossy fiber terminal integration during adult neurogenesis. Eneuro, 7(3).