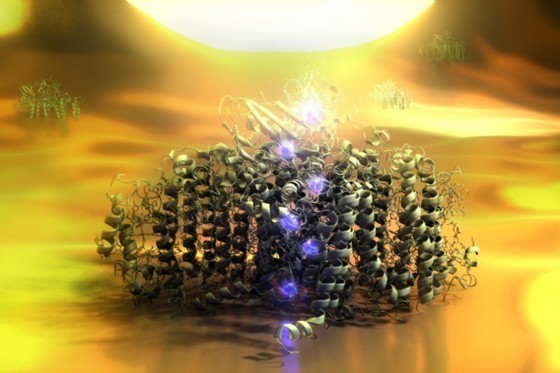
 光合作用(photosynthesis)讓植物將光轉換成化學能。利用此過程來產生電能是一個世界級的研究目標。現在,(德國)Technische Universitaet Muenchen 以及(以色列)Tel Aviv University 的科學家團隊已成功直接追溯並測量由單組光系統 I(photosystem I)分子所產生的光電電流(photoelectric current,譯註:一般簡稱光電流)。
光合作用(photosynthesis)讓植物將光轉換成化學能。利用此過程來產生電能是一個世界級的研究目標。現在,(德國)Technische Universitaet Muenchen 以及(以色列)Tel Aviv University 的科學家團隊已成功直接追溯並測量由單組光系統 I(photosystem I)分子所產生的光電電流(photoelectric current,譯註:一般簡稱光電流)。
一支由 Joachim Reichert、Johannes Barth 與 Alexander Holleitner(Technische Universitaet Muenchen)以及 Itai Carmeli(Tel Aviv University)所領導的科學家團隊,開發出一種方法來測量單一功能化光合作用蛋白質系統的光電流。科學家能證明這樣一個系統能在人造光伏裝置結構中被整合並被選擇性地處理(selectively addressed),同時保留其生物分子的功能性特性。這些蛋白質代表光驅動、高效率單分子電子幫浦,能成為奈米級電子電路的電流產生器。這個跨學科團隊將這些結果發表在 Nature Nanotechnology。
科學家研究 光系統-I 的反應中心,是一個葉綠素蛋白複合體(chlorophyll protein complex)位於藍綠菌(cyanobacteria,藍菌,譯註:原稱「藍綠藻、藍藻」,因無細胞核,故最近被歸入「細菌域」)葉綠體(chloroplasts)的膜上。植物、藻類與細菌利用光合作用將太陽能轉換成化學能。此過程的起始階段 — 在此光被吸收且能量與電子被轉移 — 是由葉綠素與類胡蘿蔔素(carotenoid)複合物所組成的光合作用蛋白質所斡旋。直到目前為止,沒有任何一種方法夠敏感,足以測量單個蛋白質所產生的光電流。光系統-I 展現出優異的、只在光合作用系統中出現的光電特性。奈米尺度的大小,更進一步使 光系統-I 成為分子光電學( molecular optoelectronics)中一種有希望的應用單元。
物理學家得要精熟的第一個挑戰是開發出一種方法,在電氣上(electrically)接觸位於強光場中的單組分子(single molecules)。此實體化奈米裝置的中央元素由光合成蛋白自組裝而成,並透過共價方式利用半胱胺酸突變基(cysteine mutation groups)與金電極鍵結。光電流透過部屬在掃描式近場光學顯微鏡設置中的包金玻璃尖端(gold-covered glass tip)來測量。光合作用蛋白在光學上受到經引導通過四面體尖端(tetrahedral tip,那在同一時間提供電接觸)的光通量所激發。利用此技術,物理學家能在單組蛋白質單位中監測光電流產生。
資料來源:Solar cell consisting of a single molecule: Individual protein complex generates electric current. phys.org [October 2, 2012]
轉載自 only perception