中央研究院生物醫學科學研究所研究員謝清河、羅傅倫(Dr. Roffler, Steve R.)研究團隊,成功開發「具導航能力且可重複投遞之新型標靶藥物輸送系統」,藥物、幹細胞或血管生長因子得以精準輸送至人體患部,能促進心血管疾病患者的心血管再生。
此項技術將為糖尿病引發的下肢缺血患者帶來福音,也可望應用於癌症治療。研究成果 2016 年 11 月 16 日刊登於國際頂尖期刊《科學轉譯醫學》(Science Translational Medicine),並被選為重點論文,向世界主要媒體發文介紹。

中研院生醫所研究員,同時也是臺大醫院心血管外科醫師謝清河表示,目前心血管疾病高居全球死亡率第一位。以心肌梗塞為例,心肌細胞在缺血幾個小時內便會大量死亡,即使以溶血栓藥物或心導管介入性治療,也無法恢復正常功能。此外,糖尿病患者與高血壓、高膽固醇的族群常因血管阻塞造成下肢缺血,導致病人無法行走、傷口癒合不良,到最後甚至必須截肢。
謝清河說,人類心血管組織再生不易,即使利用藥物或細胞治療,也無法專一、持續將藥物注射至治療部位。組織再生過程十分複雜,不僅需要多種血管新生因子,每種因子在血管新生的各步驟中皆扮演不同角色,其有效作用的時間長短不一、發生作用的細胞又不同、作用機制也大相逕庭。一個可行的方式是,模擬血管新生的節奏,進行階段性的藥物、生長因子或幹細胞治療。
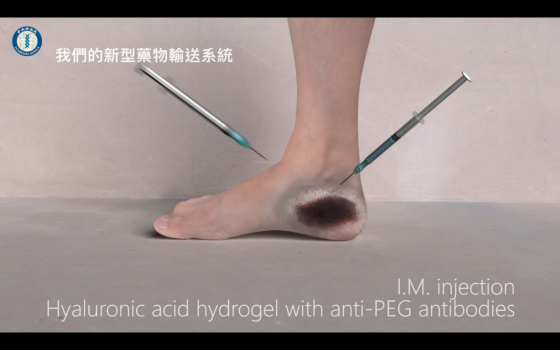
謝清河團隊利用「抗體與受體具專一性結合」的概念,將由羅傅倫團隊所研發的抗聚乙二醇(anti-PEG)抗體,與生物可分解之水凝膠(hydrogel)共同混合後,注射至治療部位建立「標靶」。接下來注射帶有 PEG 的藥物,經全身循環後,仍會被引導到水膠注射的標記位置,標靶將如磁鐵一般吸附藥物,讓藥物得以精準到達治療部位。
羅傅倫博士表示,通常只有少於 1% 的藥物能抵達患部,藥物也無法在患部久留。透過新型的藥物輸送系統,我們可以讓藥物維持在正確的位置,增加治療效果。

論文第一作者吳佩蓉表示,此技術歷經 4 年的研發與實驗,已成功治療老鼠及蘭嶼豬下肢缺血。以實驗老鼠為例,首先替缺血的下肢建立藥物標靶系統,再分別注射兩種不同生長因子,一個保護血管免於傷害,另一個則協助新血管的生成,療程結束後老鼠下肢的血液流量增加 40%,證明該技術確能協助血管新生。
謝清河強調,此技術可提升多種藥物的標靶治療,並降低藥物使用劑量,減少對其他健康組織的毒性。期待此技術能盡快進行臨床試驗,未來將幫助心血管疾病患者;藥物傳輸平台也可望應用於癌症治療,藉由提升藥物的療效,減少副作用發生。
他補充,近年許多研究致力發展多重蛋白質藥物療法,或經由連續給藥的方式治療心血管疾病,可惜成效仍十分有限。新藥開發、創新醫材,或發展治療心血管疾病之細胞療法,都需要仰賴有效的藥物傳輸系統,這項再生醫學的科技突破,將可促使相關研究加速前進。
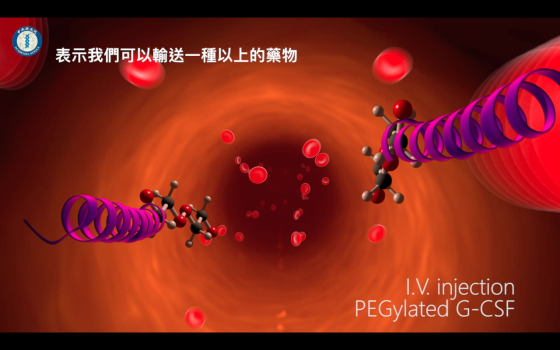
論文第一作者為本院生醫所前研究助理吳佩蓉,除本院生醫所與應科中心之外,團隊成員還包括美國西雅圖華盛頓大學三位教授。研究經費則由科技部、衛生福利部、財團法人台灣生技醫藥發展基金會及中央研究院支持。
該論文已於美東時間 11 月 16 日刊載於期刊《科學轉譯醫學》(Science Translational Medicine),文章標題為Reloadable Multi-Drug Capturing Delivery System for Targeted Ischemic Disease Treatment。
- 研究成果示意動畫
(本文改寫自中研院媒體小組新聞稿)