文/彭琬馨
你身邊有漸凍症、失智症、自閉症的朋友嗎?
雖然目前醫療科技發達,我們對於這類神經元退化造成的疾病如何發生,了解的還是太少,只能靠後天醫療方式減緩病狀。但如果能找出疾病成因,是不是就能有效控制病狀發展、對症下藥?
神經元退化性疾病 神經突觸是關鍵
這些神經元退化性疾病的特徵之一,就是神經細胞用來傳遞訊號的突觸(synapse)因為病變而萎縮。突觸數量是訊息傳遞速度、準確性的重要關鍵,它就好像是螞蟻的觸角,負責和另一個細胞接觸、交換訊息。因為突觸是不同神經細胞(或肌肉細胞)傳遞訊息的連接點,突觸越多、細胞間連結越緊密、記憶就越好,反之則下降。在許多失智症患者的神經細胞上,突觸都有減少的情況。
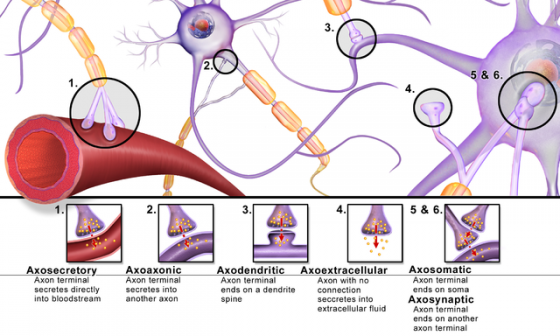
白胺酸可能是治療解方
中研院分子生物研究所研究員薛一蘋帶領研究團隊,經過五年的研究,他們發現可以透過補充一種胺基酸——白胺酸(Leucine),來增加神經細胞突觸的數量與活性。
這個方法聽起來非常簡單,但為什麼增加白胺酸就能影響突觸?
他們發現當細胞偵測到大量游離白胺酸,就會開始進行蛋白質合成,也就是說,只要簡單的增加白胺酸濃度,就能調控蛋白質生成數量的增減。

「因為大家都沒聽過這個路徑,連論文審查的委員都不太相信。」薛一蘋坦言,這個新穎機制剛提出時經過一番不小的波折,也因此更凸顯研究的重要性。不過,她也特別強調,這個方法並不是針對突變細胞進行治療,原先有缺陷的細胞也不會因此恢復正常功能,在小鼠實驗上,大約經過兩個星期,胺基酸的療效會逐漸衰退,「這樣其實是好的,我們才能夠隨時調整白胺酸數量」。
在小鼠實驗的部分,不僅可以看到突觸數量的增加,在行為實驗中,也看到很好的成效。如果能更進一步往臨床實驗邁進,應用到患者身上,或許你身邊的朋友就有可能成為受惠的那一人。更重要的是,薛一蘋告訴我們這個方法「目前看起來沒有副作用」,對患者本身不會造成其他負擔。
過去研究奠定今日成果
會有這樣的發現其實也不是偶然,薛一蘋團隊早在2011年就發現,細胞中一種蛋白質——「纈絡胺酸蛋白質」(valosin-containing protein)的突變,會造成突觸數量減少,卻不知道其中的機制是什麼。直到近期的研究發現,這個蛋白質透過影響細胞中掌管蛋白質生成的大本營「內質網」,造成它產生的蛋白質數量就大幅下降,也影響到了突觸的數量和活性。
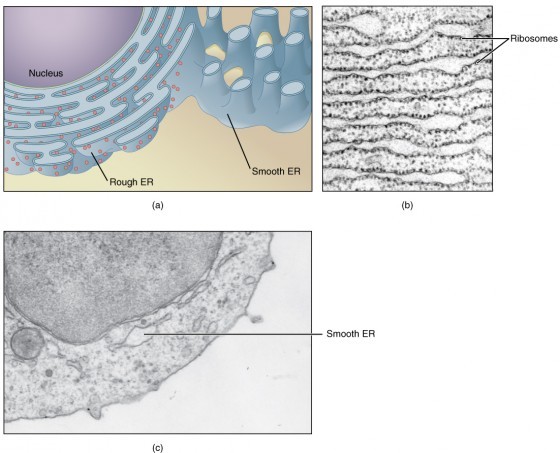
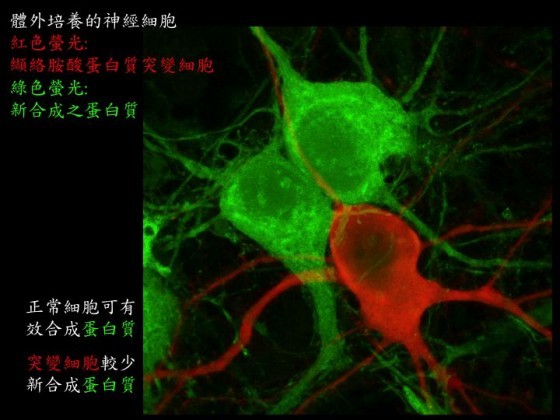
此外,2014年,研究團隊就曾發表自閉症致病機制的相關論文,這個研究證實,自閉症的其中一個致病基因 T-brain-1 (簡稱TBR1)的缺失,會讓大腦喪失一種名為「後段前連合」(posterior part of anterior commissure,負責聯絡兩個大腦半球的杏仁核)的特定結構,導致訊息無法正確傳送,由於杏仁核掌管大腦社交活動、情緒反應等功能,具有 TBR1 缺失的小鼠,在行為上也出現缺陷。影響自閉症的基因非常多,連帶增加後續治療的困難度,了解致病原因後,也較能對症下藥。
面對像是自閉症、漸凍症和失智症等神經退化性疾病,仍有許多未知等待解決,薛一蘋團隊所發現「增加白胺酸」的療法,也尚在動物研究階段。有待這些研究幫助我們了解這些疾病,也讓應用在人類患者的治療變成可能。


































