流言: 【刮腋毛易導致乳腺癌】因為腋毛幫助汗液排除,沒有腋毛會使得毒素的排除受阻是毒素儲存於淋巴結,從而提高罹患乳腺癌的幾率。乳腺癌在腋窩區域發病最多也是由此造成。
真相: 夏日將至,很多女孩都會選擇刮腋毛,因為在她們看來吊帶背心下竄出鬱鬱蔥蔥的腋毛是不可接受的事情。不過網絡上卻流傳著「刮腋毛易導致乳腺癌」的說法,這個警告乍看起來頭頭是道,但只要仔細分析一下就不難發現它其實漏洞百出。
排毒?和排汗完全無關嘛
不少流言的慣用伎倆都是首先提出一個虛假的前提,然後用看似正確的邏輯推理得出一個錯誤的結論,例如這則流言就首先認定「排汗受阻會導致排毒受阻,最終導致癌症發生」。
在現代醫學裡很難為「排毒」找到合適的定義。如果將致癌物質認為是「毒」,那麼我們身體內大多數毒素都是由血液運輸到肝臟或腎臟代謝清除的。這些「毒素」或經由膽汁隨糞便排出或通過尿液排出體外[1]。流言中提到的「膝蓋後方關節、耳後、腋窩等主要排毒區域」實在是無從談起。
除了肝腎之外,淋巴結負責消滅體內細菌或其他病原體,同時也能清除部分對身體健康有危害的物質。但淋巴結清除「毒素」的機制不是出汗而是免疫運送的,代謝產物通過淋巴回流最終也是進入血液系統的[2]。實際上,淋巴結根本不與汗腺直接連接。汗腺存在於皮膚之中,而非淋巴結內。
排汗是人體正常的生理過程,它可以調節體溫、保持皮膚濕潤,同時排出極少量代謝廢物。不過汗液的99%以上都是水,剩餘極少部分溶質包括礦物質、乳酸、尿素及其他極微量的代謝產物。這些溶質中絕大多數來源於血漿,但濃度遠低於尿液[3][4],因此所謂出汗的「排毒」作用十分有限,局部排汗受阻很難對人體代謝造成顯著影響。
阻礙排汗?刮腋毛無罪
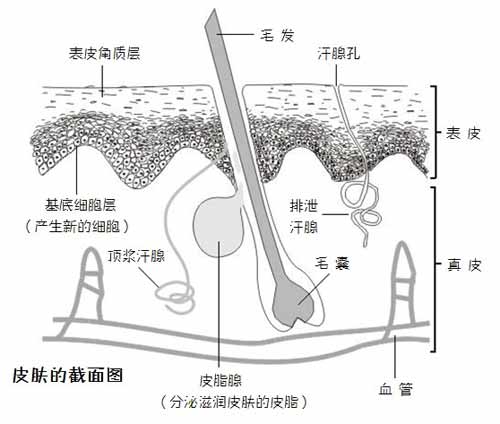
「刮腋毛會使得排汗受阻」是流言中所認定的另一個「事實」。但實際上,從毛囊結構(見下圖)上不難發現,刮腋毛並不會影響汗腺的結構,也不會阻礙排汗。
當然,需要提醒的是,對於採用物理方式刮除腋毛的人來說,如果因為刮腋毛不當造成皮膚的破損,確實容易引起感染、毛孔阻塞,有可能對排汗造成一定影 響。所以,最好使用清潔鋒利的剃毛工具,剃毛前充分濕潤並適當使用潤滑產品對避免劃破皮膚也有幫助。同時切記不要與他人共用剃毛工具。
腋窩淋巴結與乳腺癌
流言還聲稱幾乎所有的乳腺癌都是發生在乳房外側上方的區域,因為這裡是排毒淋巴結的所在地。臨床上以乳頭為原點,畫橫縱軸將乳房分為四個象限,外上 象限乳腺癌原發灶發病率確實最高,美國癌症協會(American Cancer Society)對此的解釋是,這很可能只是因為該像限乳腺組織最多而已,其發病比例和乳腺組織在外上象限分佈的比例類似,和淋巴無關[1]。
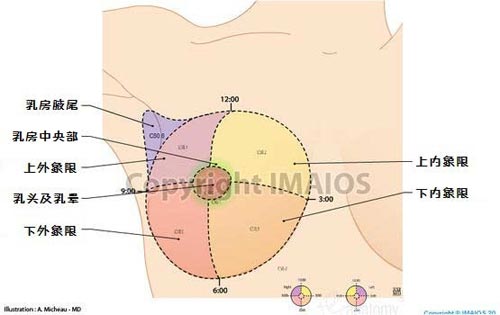
值得一提的是,腋窩淋巴結與乳腺癌的淋巴轉移(注意,不是原發癌灶)確實有密切的聯繫。乳腺癌淋巴結轉移大多都發生在腋窩淋巴結,但這依然與所謂的「腋窩淋巴結儲存毒素」無關,而是由乳腺淋巴回流途徑決定的。
乳腺周圍分佈著眾多淋巴結,乳房組織產生的大部分淋巴液都是經胸大肌外側緣淋巴管先流至腋窩淋巴結,再流向鎖骨下淋巴結。因此大部分的乳腺癌淋巴轉移也都發生在腋窩淋巴結[8]。
結論:謠言粉碎。 刮腋毛導致乳腺癌的謠言無論在論據還是結論上都是站不住腳的。目前並無臨床證據支持刮腋毛會致乳腺癌,也無研究表明乳腺癌發病位置同刮腋毛有關。刮腋毛在審美上是好是壞因人而異,但依據目前的醫學認識,選擇刮腋毛的人不必擔心會對乳腺健康帶來負面影響。
作者吐槽:「男人之所以比較不會得乳腺癌的原因是他們從未剃掉腋毛」恐怕是謠言裡最無厘頭的論據了。乳腺癌的發生受到遺傳、外部環境、乳腺組織含量,雌激素等多方面的影響,這些因素對男女都有作用。男性乳腺組織含量遠小於女性是男性較少患乳腺癌的主要原因。罹患會 導致體內雌激素大量分泌的疾病的男性,其乳腺癌發病率也會大大增高[1]。一些含有可能影響雌激素代謝物質的化妝品也因此被質疑。
參考資料
- American Cancer Society: Antiperspirants and Breast Cancer Risk
- wikipedia: Lymph node
- Czarnowski, D., et al., Plasma ammonia is the principal source of ammonia in sweat. Eur J Appl Physiol Occup Physiol, 1992. 65(2): p. 135-7.
- Cizza, G., et al., Elevated neuroimmune biomarkers in sweat patches and plasma of premenopausal women with major depressive disorder in remission: the POWER study. Biol Psychiatry, 2008. 64(10): p. 907-11.
- wikipedia: Sweat gland
- wikipedia: Apocrine sweat glands
- Kohoutova, D., A. Rubesova, and J. Havlicek, Shaving of axillary hair has only a transient effect on perceived body odor pleasantness. Behavioral Ecology and Sociobiology, 2012. 66(4): p. 569-581.
- 吳在德 主編 《外科學》第五版,人民衛生出版社 2000年
轉載自科學松鼠會,作者林竹蕭蕭。本文首發於果殼網「謠言粉碎機主題站」《刮腋毛易導致乳腺癌嗎?》






































