來解析大腦吧!
近年來想要瞭解大腦所做的嘗試,主要是將大腦分解為各個組成部分,然後各自檢驗這些部分,再將它們納入一個更大的理論框架中——此即哲學上的化約論(reductionism)。雖然許多人相信現在該丟棄這種思考方式,因為科學已證明大腦是比各部分的總和更為複雜,但化約論為我們提供了大量知識,許多治療阿茲海默症的研究即是仰賴這些知識。
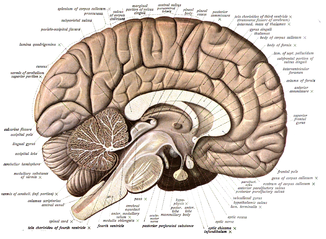
廣泛來說,大腦主要是由兩種細胞類型所構成——神經元與神經膠質。神經元,即大腦的神經細胞,是一種放電細胞,它會利用名為突觸的特殊接觸點,互相傳送化學訊息。它們經常被比喻為茂密森林中的樹,或是電信網路中的電線。你也可以把它們想成社群媒體中的名人:每個神經元就有如擁有約八百五十億「 朋友」的人,而它們只是多達百兆突觸連結的「 網路」之一部分。這意味著在你腦中的最深處,每一秒便有數十億的神經元正傳送著數兆個突觸訊息。
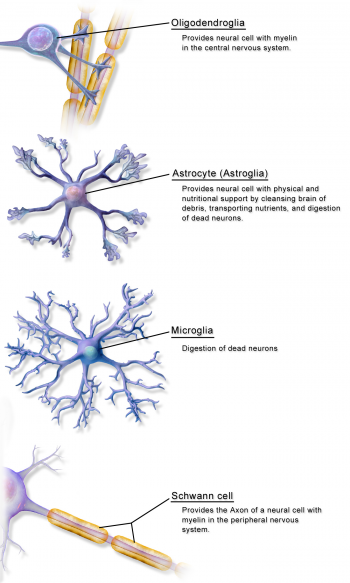
神經膠質(glia,希臘文的膠)乃是保護與支持神經元的不帶電細胞。過去被認為不具有太多其他作用,因此有此貶抑的希臘文翻譯。但現在有很好的證據顯示神經膠質在大腦中扮演著更傑出的角色,而站在阿茲海默症研究最前線的眾多神經科學家,正忙著破解這些角色,試圖將它們運用在治療上。
根據英國生物學家路易斯.沃爾伯特(Lewis Wolpert)的說法,理解神經元複雜性的最佳方式,便是將每個神經元想像成一個成人大小。以此比例,整個大腦將涵蓋十公里的區域,接近曼哈頓的大小,並且朝向天空十公里遠。曼哈頓的人口大約一百六十萬人,大腦空間則是由數十億的「 神經元人」一個個向上堆疊,每個人會與一百到一千個之間的鄰居交談。如果你可以想像這個畫面,便能體會神經元是多麼複雜。
想了解阿茲海默症,得先了解神經元
典型的神經元是由細胞體、名為樹突(dendrites)的無數細小突起,以及一個名為軸突(axon)的長型突起所組成。而細胞體內存在多個「 內部器宮」,或稱為細胞器——例如存放神經元 DNA 的細胞核(nucleus)、提供神經元能量的粒線體(mitochondria)以及扮演微小蛋白質工廠的核糖體(ribosomes)。沿著樹突長條緊密排列的是突觸,每個突觸透過幾乎碰觸到其他神經元軸突(axon)的終末(terminal)來與其他神經元相互連繫。以此方式,神經元便形成固定但高度動態的互動網。
那是在一九七八年,幾乎同時來自不同英國生物化學家團隊的三項突破性研究,改變了阿茲海默症研究的面貌:其中一項是由愛丁堡大學的彼得.戴維斯(Peter Davies)所主導;第二項為紐卡索大學的伊萊恩(Elaine)和羅伯特.佩里(Robert Perry)主導;第三項則為倫敦神經學研究所的大衛.鮑恩(David Bowen)所主導。

一九七○年代是對失智症認識最豐碩的十年。在美國,傑出的健康活動推廣家佛羅倫斯.馬奧尼(Florence Mahoney),開始遊說政治人物建立一個專精於年齡相關疾病的新機構,以補充既有國立衛生研究院(NIH)的不足。在她的協助下,國會說服尼克森總統於一九七四年通過「 老化研究法案」(Research on Aging Act),並建立了「 國家老齡研究所」(NIA)。在英國,健康活動推廣家彼得.坎貝爾(Peter Campbell)創立了「 精神病人」聯盟(MPU),致力於消除當時療養院式的精神病系統—這在當時都是不斷揭露疏於照顧並虐待失智症病人的來源,而在一九七九年,一小群病人家屬與謹慎的醫療從業人員組成了阿茲海默症協會(即今日的阿茲海默症協會)。 在歐洲的柏林、巴黎、羅馬與斯德哥爾摩等地著名的學術機構,亦開始集結不同背景的科學家,並且建立以挖掘阿茲海默症未知來源為唯一目標的大學科系。
分娩麻醉為何會失去記憶?
在英國,有一位生物化學家注意到分娩麻醉效果和記憶形成之間具有神祕的連結。在那時,採用一種名為東莨菪鹼(scopolamine)的藥物來減輕孕婦生產時的疼痛。在此之前,氯仿(chloroform)是唯一選擇,但因為它是具生命威脅的併發症如心臟衰竭的來源,因此醫療機構飽受指責。而東莨菪鹼取自亞洲的開花植物山莨菪(Scopolia tangutica),其改良之處在於它具有誘發「 半麻醉狀態」(Twilight Sleep)的能力:病人不會感到疼痛,但同時能保持完全清醒。然而令人驚訝的是,他們發現一項有趣的觀察,產婦在生產後對於生產過程完全沒有記憶。沒人能解釋原因。科學家知道的只有東莨菪鹼會干擾神經系統中乙醯膽鹼的信號傳導。

記憶和乙醯膽鹼的關係是?
要想弄清楚神經化學如何影響記憶的形成以及保存,對神經科學來說仍有如聖杯般的存在。我們仍不知道記憶是如何運作的。一九七○年代,挪威科學家皮爾.安德森(Per Anderson)與泰耶.勒莫(Terje Lømo)提出了至今仍最具說服力的理論,主張記憶的製造與喪失,是神經突觸個別強化與變弱所致。他們稱此模型為「 長期增強作用」(LTP)。他們表示,此現象的發生,是在一突觸接收到高頻電流的刺激,而這會造成兩神經元之間連結的強度持久增強。這幾乎就像科學中的所有事物一樣,事實(或此例的假設)總是奇怪到難以理解,但安德森與勒莫提出這些連結簡單來說「 就是」我們的記憶。這與我們感知到的——傳送至我們大腦的影像與感覺——完全不同。記憶實際上是經過編碼的。
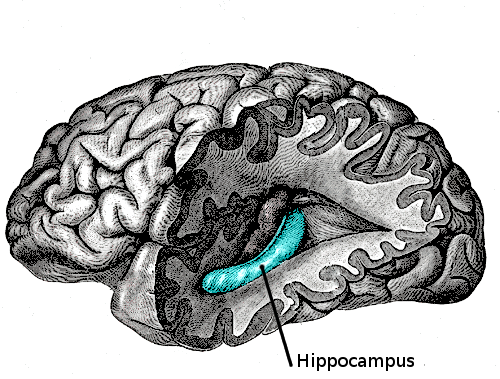
因此,當一段記憶產生時,例如初次與某人會面,這個資訊首先會傳送到海馬迴,以在突觸網路中進行編碼。這個資訊有些會停留在此成為短期記憶,大約維持個三十秒,但如果這個會面有某些重要事情或強烈情感元素存在,那麼這個資訊就會導入皮層的突觸,在那裡儲存為長期記憶。這個科學理論聽起來或許不太精確且無法令人滿意,但這就是我們僅能做的推論。我們知道長期記憶廣泛來說可以分為陳述性記憶和程序性記憶。陳述性記憶指的是一生中收集的知識,例如家中小狗的名字或你有幾個小孩等等。程序性記憶則牽涉到如何執行某些事,例如綁鞋帶或開車。但若就記憶的神經生理學角度來說,安德森與勒莫的 LTP 理論,再結合以某種方式涉入的神經傳遞物信號發送,仍是(目前亦是)神經科學中對記憶最佳的描述。
對此理論,英國生物化學家馬上提出一個明顯的問題:
乙醯膽鹼的流失有可能是造成阿茲海默症記憶衰退的原因嗎?
這是個十分有趣的理論。如果證實為真,或許可將整個謎團縮小至單一問題:科學家便能開發一種只取代乙醯膽鹼的新藥。確實,帕金森(Parkinson’s)的研究在一九六○年代便是以此種方式取得勝利,當時發現帕金森症患這會喪失神經傳遞物多巴胺(dopamine),而科學家們便發明一種方式,使用左旋多巴(Levodopa)藥物來取代它。雖然不見得能治癒,但對帕金森患者的治療成效一直不錯。
以人為方式增進大腦的記憶能力
但以阿茲海默症的情況來說,答案並不是那麼直接,此想法的成功與否取決於數個問題。首先,從已故阿茲海默症病患取得的大腦樣本中,是否發現減少了乙醯膽鹼?在對屍體解剖組織一番密集的搜尋後,各英國團隊取得一致意見,並在一九七八年紛紛發表他們的發現。看起來「 是的」。
下一個問題是,若以人為方式在年輕健康的人身上阻擋乙醯膽鹼,是否會觸發和老年人身上所見的相同記憶喪失問題?幸運的是這個問題已有答案。一九七四年,芝加哥西北大學的大衛.德雷切曼(David Drachman)與珍妮特.萊維特(Janet Leavitt)針對一群年輕學生志願者,讓他們服用以東莨菪鹼製成的「 半麻醉劑」,並測試他們儲存與吸收新記憶的能力。例如他們是否在聽完錄音機播放的一串隨機數字後,能記住並重複它們?以及他們能列出多少類別為動物、水果以及女孩名字的名詞?接著,他們又針對五十五歲到八十九歲之間未服用藥物的健康志願者進行同樣的測試。令人驚訝的是,在每個測試中未服藥學生的表現遠遠超過年長測試者,而在東莨菪鹼影響下的學生則表現得和年長對手們一樣糟。在此,再次得到肯定的答案。

最後一個也是最重要的問題:
是否提高阿茲海默症患者腦中的乙醯膽鹼釋放,便能增進他們的記憶力?
測試此問題最簡單的方式是透過飲食。若要製造乙醯膽鹼,神經元首先需要膽鹼,這是一種在血液循環中發現的維他命。這種維他命從我們吃的食物中即可大量提供——例如蛋、牛肉以及魚即富有大量膽鹼。
——本文摘自《當大腦開始崩壞:科學 X 人性 X 歷史,人類對阿茲海默症的奮戰》,2018 年 6 月,八旗文化。




































