吸血鬼的故鄉外凡尼西亞(Transylvania)一直以來都是羅馬尼亞的文化重鎮,位於此處的哈澤格(Hațeg)不僅是充斥著中世紀古老建築與教堂的文化古城,也是孕育了當代化石生物學的搖籃。
此地的旦蘇修拉組(Densuș Ciula Formation)地層出土了不少恐龍化石,白堊紀末期的東歐地形相當破碎,當時的哈澤格是眾多島嶼當中較大的一座。出身奧匈帝國的古生物學家諾普查男爵(Franz Nopcsa)便是在此研究晚白堊紀的動物相,而得出了島嶼動物可能因為適應外在環境而產生「侏儒化」的現象,這個假說也在後來的島嶼生物學當中得到驗證。

然而,晚白堊紀的哈澤格島有個有趣的現象,那就是從有紀錄以來,至今人們從未在當地採集到大型獸腳類出現過的蹤跡,就連任何一顆牙齒也沒有,這絕對是個非比尋常情況。對於這個不尋常的現象,英國的古生物學家戴倫奈許(Darren Naish)和翼龍專家馬克維頓(Mark Witton)可能有個驚人的解釋:
「在當地佔有頂級掠食者這個棲位的並不是恐龍,而是一種大型的翼龍!」
壯碩卻仍所知甚少的神龍翼龍科
神龍翼龍科(Azhdarchidae)是一群生活於白堊紀末期極為特殊的動物,這個類群的翼龍有些體型異常的巨大,有些展翼長可超過 10 公尺、重達 220 公斤,猶如賽斯納(Cessna)的單引擎飛機。比較知名的諾氏風神翼龍(Quetzalcoatlus northropi)便是屬於這個類群。
這些翼龍經常被描述得相當壯觀、且有個細長的脖子,還有一個不帶有牙齒的喙。即便他們經常因為巨大的體型而成為電視或電影中的常客,但其實目前科學家仍對這些動物所知甚少,出土的化石也因為他們的身體結構不易保存,所以經常只有局部的零碎骨頭被發現。
另一種神龍翼龍科的化石於 1991 年在哈澤格盆地中被發現,因為這些骨骼相當的壯碩,起先被認為是屬於獸腳類恐龍所有。直到 2002 年,法國古生物學家巴佛陶(Eric Buffetaut)與他的同事才將這些化石鑑定為─怪物哈特茲哥翼龍(Hatzegopteryx thambema),並以希臘文「可怕的怪物」做為種小名來描述牠龐大的體型。

正如同其他的神龍翼龍科成員,哈特茲哥翼龍出土的化石也相當破碎,編號 FGGUB R 1083A 的正模標本包含了一段嚴重損壞的左肱骨和一部分後半段的頭顱骨;另外同一地層中還有一段巨大的股骨,標本編號 FGGUB R1625,據信也屬於哈特茲哥翼龍所有。
根據這些已知的素材推估,哈特茲哥翼龍展翼長約10至12公尺。哈特茲哥翼龍的骨骼上有不尋常的增厚,這樣的厚重、結實的解剖特徵在翼龍身上相當罕見;為了減低飛行所需的負擔,哈特茲哥翼龍的肱骨和頭骨都有像海綿般內部空洞化的結構。
哈特茲哥翼龍最驚人的地方莫過於牠的頭部結構,牠的頜關節具有獨特的溝槽,能使牠們的嘴巴張得更開,巴佛陶等人根據現有的顱骨部分推估哈特茲哥翼龍的吻部竟然寬達 50 公分,整個頭骨很可能長達三公尺。即使是由維頓在近年較為保守的估算,哈特茲哥翼龍仍是頭顱骨最長的非水生動物。
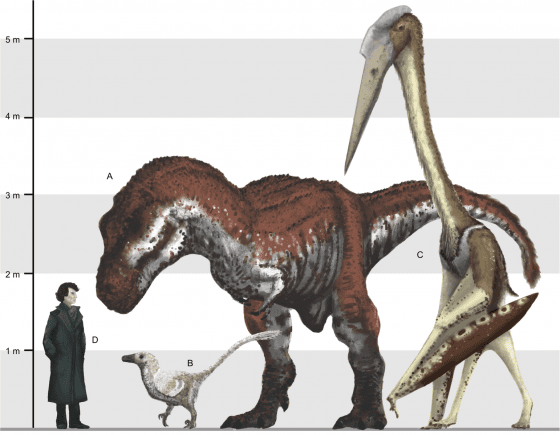
但是像翼龍這樣身體結構輕巧易碎的動物,真的有可能是主宰晚白堊紀東歐諸島的頂級掠食者嗎?
哈特茲哥翼龍與其他神龍翼龍科超級比一比
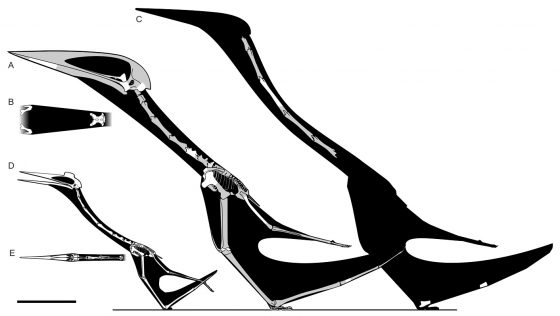
為了更加瞭解哈特茲哥翼龍在獨特的解剖結構,奈許和維頓比較了各種神龍翼龍科的頸部骨骼。
其他大型的神龍翼龍科成員─風神翼龍與阿氏翼龍(Arambourgiania)的頸部顯得相當纖細而脆弱。阿氏翼龍是另一種出土於約旦的神龍翼龍科,模式標本是一段長達75公分的頸部骨骼,也因為這段骨骼長的驚人,最初被描述時還被誤認為是翼骨的一部分。根據推測阿氏翼龍的頸部總長度可達2公尺,雖然知名度不及風神翼龍,但他的體型很可能比風神翼龍更為巨大,甚至可能是目前已知最大的翼龍類。

而這樣的特徵更襯托出了哈特茲哥翼龍頸部結構的獨特性,對比於風神翼龍與阿氏翼龍這兩種一般認知中神龍翼龍科的典型,哈特茲哥翼龍的頸部顯得較短,且更為厚實粗曠。
編號 EME 315 的骨骼,是由維米爾(Mátyás Vremir)在 2010 年所描述一塊出土於哈澤格地區的神龍翼龍科頸部骨骼,同時也是目前唯一一塊屬於哈特茲哥翼龍脊椎部分的素材。透過測量這塊骨骼,奈許和維頓認為細長的頸部顯然不是神龍翼龍科共有的解剖特徵。事實上,近年發現更多新出土的神龍翼龍科化石也顯示,這些動物可能遠比我們過去想像中的更多樣。
根據這兩種大型神龍翼龍科不同的頸部結構,奈許與維頓認為牠們很可能在各自的生態系當中扮演著截然不同的角色。

長頸的阿氏翼龍和風神翼龍由於頸部可彎曲的範圍小、且較少有肌肉附著,牠們可能傾向選擇較小型的獵物。畢竟高強度的狩獵行為會增加對其頸部所需的應力,而牠們纖細的頸部可能無法承受這樣的壓力。
頸部較短而強壯的哈特茲哥翼龍則具有完全不同的捕食策略,由於頸部有厚實的骨骼、強健的肌肉附著以及寬闊的吻部,根據這些特質,哈特茲哥翼龍絕對是一種比阿氏翼龍更為結實的動物,且更能應付各種高強度的格鬥,甚至能輕易的捕食體型較大的動物。
也許這解釋了為何一個多世紀以來科學家從未能在哈澤格的旦蘇修拉組找到任何大型的獸腳類出沒的痕跡,因為自白堊紀末期的森諾曼階(Cenomanian)至馬斯垂克階(Maastrichtian),哈澤格島一帶的島嶼地形相當破碎,對大型的獸腳類恐龍來說,環繞在四周的海洋根本就是天然屏障,但是要越過這些水域對哈特茲哥翼龍簡直易如反掌,也無怪乎此處找不到大型獸腳類恐龍的蹤跡。
在這裡,哈特茲哥翼龍就像德古拉伯爵一樣俯瞰他統治的領土。
參考資料
- Naish D, Witton MP. (2017) Neck biomechanics indicate that giant Transylvanian azhdarchid pterosaurs were short-necked arch predators. PeerJ 5:e2908. DOI:10.7717/peerj.2908
本文轉載自作者部落格:PREHISTORIC BEASTS ,歡迎追蹤作者粉絲頁:遠古巨獸與他們的傳奇






























